
(12分)尖晶石型锰酸锂(LiMn2O4)是一种环保绿色能源新型材料。实验室通过下列方法制取:将MnO2和Li2CO3按4︰1的物质的量比配料,球磨3~5小时,然后升温至600℃~750℃,保温24小时,自然冷却至室温得产品。
(1)保温24小时的目的是____________________________________________________。
(2)写出该反应的化学方程式_________________________________________________。
(3)实验室测定锰酸锂中锰的平均化合价的实验步骤如下:
步骤1:准确称取0.1g左右的尖晶石型锰酸锂试样于锥形瓶中,加入5mL稀硫酸、10.00mL 0.2000mol/L草酸钠(Na2C2O4)标准溶液,于80℃水浴加热溶解;
步骤2:待试样全部溶解,立即用浓度为0.2000mol/L的高锰酸钾溶液滴定至终点;
步骤3:计算样品得电子的物质的量n;
步骤4:将溶液中Mn2+氧化为Mn3+,再用硫酸亚铁铵标准溶液滴定,记录实验数据,计算出样品中Mn元素的质量为m;
步骤5:将实验步骤1-4重复2次。
已知反应: 2Mn3++C2O42-=2Mn2++2CO2↑;Mn4++C2O42-=Mn2++2CO2↑
2MnO4-+5C2O42-+16H+="2" Mn2++10 CO2↑+8H2O
①步骤2中,为判断滴定终点,_________(填“需要”或“不需要”)加入指示剂。
②步骤4中,滴定时盛放硫酸亚铁铵标准溶液的玻璃仪器是___________________。
③请用样品得电子的物质的量n和样品中Mn元素的质量m来表示样品中Mn元素的化合价=_____。
(1)MnO2与Li2CO3充分反应。
(2)8MnO2 + 2Li2CO3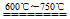 4LiMn2O4 + 2CO2↑ + O2↑。
4LiMn2O4 + 2CO2↑ + O2↑。
(3)①不需要。 ②酸式滴定管。 ③。
解析试题分析:(1)保温24小时的目的是让MnO2与Li2CO3充分反应。(2)MnO2和Li2CO3反应后只有Mn的价态降低,必然有元素的化合价升高,C元素处在最高价态,不能升高,则只能是O元素价态升高,所以还有O2生成。该反应的方程式为:8MnO2+2Li2CO3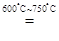 4LiMn2O4 + 2CO2↑ + O2↑。(3)①因为KMnO4本身有颜色,所以不需要指示剂。②硫酸亚铁铵溶液水解呈酸性,所以要用酸式滴定管盛放。③设Mn元素的化合价为x,则n=
4LiMn2O4 + 2CO2↑ + O2↑。(3)①因为KMnO4本身有颜色,所以不需要指示剂。②硫酸亚铁铵溶液水解呈酸性,所以要用酸式滴定管盛放。③设Mn元素的化合价为x,则n=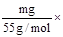 (x-2),x=2 + 55n/m。
(x-2),x=2 + 55n/m。
考点:化学实验习题
点评:本题看似复杂,但是问题比较简单,只要掌握基本知识就可以解答。


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
 (2009?淮安二模)锰酸锂离子蓄电池是第二代锂离子动力电池.它的问世使得锂离子动力电池在纯电动汽车与混合动力车等大型蓄电池应用领域占据主导地位.电池反应式为:Li1-xMnO4+LixC=LiMnO4+C,下列有关说法不正确的是( )
(2009?淮安二模)锰酸锂离子蓄电池是第二代锂离子动力电池.它的问世使得锂离子动力电池在纯电动汽车与混合动力车等大型蓄电池应用领域占据主导地位.电池反应式为:Li1-xMnO4+LixC=LiMnO4+C,下列有关说法不正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
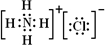
查看答案和解析>>
科目:高中化学 来源: 题型:
锂电池由于其安全可靠的性能,体积小、质量轻、高效能及可逆等卓越品质被广泛应用于移动电话、笔记本电脑、数码相机等便携式电子器材中。下图为锂电池工作原理图,阴极材料由LiMO2(M=Co,Ni,V,Mn)构成,阳极材料由石墨构成,阴、阳两极之间用半透膜隔开,充电时锂离子由阴极向阳极迁移,放电时则相反,电池可表示为:
(-)Cn/LiClO4/LiMO2(+)
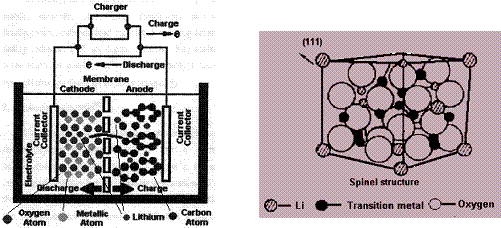
⑴ 写出锂电池充放电时的可逆电极反应。
⑵ 根据上图所示的LiMO2的尖晶石结构,写出氧的堆积方式,并指出Li和M占据何种空隙,画出以氧为顶点的一个晶胞。
⑶ 锂离子在阳极与石墨形成固体混合物,试推测并画出锂离子嵌入石墨的可能结构。
⑷ 早期的阳极材料用的是锂金属,试指出锂金属作阳极材料的不足,并说明还可以用什么物质替代石墨作阳极材料?
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省高三上学期期中考试化学试卷(解析版) 题型:实验题
(12分)尖晶石型锰酸锂(LiMn2O4)是一种环保绿色能源新型材料。实验室通过下列方法制取:将MnO2和Li2CO3按4︰1的物质的量比配料,球磨3~5小时,然后升温至600℃~750℃,保温24小时,自然冷却至室温得产品。
(1)保温24小时的目的是____________________________________________________。
(2)写出该反应的化学方程式_________________________________________________。
(3)实验室测定锰酸锂中锰的平均化合价的实验步骤如下:
步骤1:准确称取0.1g左右的尖晶石型锰酸锂试样于锥形瓶中,加入5mL稀硫酸、10.00mL 0.2000mol/L草酸钠(Na2C2O4)标准溶液,于80℃水浴加热溶解;
步骤2: 待试样全部溶解,立即用浓度为0.2000mol/L的高锰酸钾溶液滴定至终点;
步骤3: 计算样品得电子的物质的量n;
步骤4:将溶液中Mn2+氧化为Mn3+,再用硫酸亚铁铵标准溶液滴定,记录实验数据,计算出样品中Mn元素的质量为m;
步骤5:将实验步骤1-4重复2次。
已知反应: 2Mn3++C2O42-=2Mn2++2CO2↑;Mn4++C2O42-=Mn2++2CO2↑
2MnO4-+5C2O42-+16H+=2 Mn2++10 CO2↑+8H2O
①步骤2中,为判断滴定终点,_________(填“需要”或“不需要”)加入指示剂。
②步骤4中,滴定时盛放硫酸亚铁铵标准溶液的玻璃仪器是___________________。
③请用样品得电子的物质的量n和样品中Mn元素的质量m来表示样品中Mn元素的化合价=_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com