

| A. | 6 | B. | 8 | C. | 12 | D. | 14 |
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案科目:高中化学 来源: 题型:选择题
| A. | CaO与H2O反应 | B. | CH4在O2中燃烧 | ||
| C. | NaOH溶液与H2SO4溶液反应 | D. | Ba(OH)2•8H2O晶体与NH4Cl晶体反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第IA族元素铯的两种同位素137Cs比133Cs多4个质子 | |
| B. | 元素周期表有十八个纵列,共十六个族 | |
| C. | 第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 | |
| D. | 第2周期元素从左到右,最高正价从+1递增到+7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内n(A2):n(B2):n(AB)=1:1:2 | |
| B. | 单位时间内生成2nmolAB,同时生成nmolA2 | |
| C. | 生成B的速率与生成A的速率相等 | |
| D. | 容器内气体的密度不随时间变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH=CH2+Br2→CH3CHBrCH2Br | |
| B. | CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2+H2O | |
| C. | CH3COOH+CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O | |
| D. | C6H6+HNO3$→_{△}^{浓H_{2}SO_{4}}$C6H5NO2+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

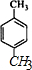
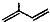 命名为2-甲基-1,3-丁二烯.
命名为2-甲基-1,3-丁二烯.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com