
 氯气是一种化学性质活泼的非金属单质,工业上可用氯气制取漂白粉、有机溶剂等.
氯气是一种化学性质活泼的非金属单质,工业上可用氯气制取漂白粉、有机溶剂等.分析 (1)①用实际参加反应的离子符号来表示离子反应的式子,在离子反应方程式中单质、气体、水应保留化学式;
②反应中盐酸中一部分氯的化合价升高,还有一部分氯的化合价不变,所以盐酸既是酸又是还原剂;
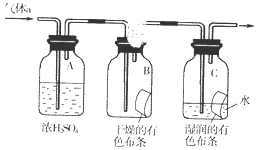
(2)①浓硫酸具有吸水性,常用作干燥剂,在实验中吸收气体中的水的作用;
②干燥氯气不具有漂白性,次氯酸具有漂白性;
③实验室用氢氧化钠溶液吸收多余的Cl2,生成氯化钠和次氯酸钠,所以离子反应为Cl2+2OH-=Cl-+ClO-+H2O;
④氯气在碱性条件下自身发生氧化还原反应,可与石灰乳反应生成氯化钙和次氯酸钙,置露在空气的漂白粉与二氧化碳、水的反应生成具有漂白作用的次氯酸;
解答 解:(1)①在4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Cl2+MnCl2+2H2O中,浓盐酸是强酸,氯化锰是盐是强电解质,都是易溶易电离的物质,拆成离子的形式,所以离子方程式为:4H++2Cl-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O,故答案为:4H++2Cl-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O;
②反应中盐酸中一部分氯的化合价升高,还有一部分氯的化合价不变,所以盐酸既是酸又是还原剂,故答案为:酸性和还原性;
(2)①制得的氯气中含有水蒸气,需要用浓硫酸干燥,所以浓硫酸的作用是除去氯气中的水蒸气,干燥氯气;
故答案为:除去氯气中的水蒸气或干燥氯气;
②干燥氯气不具有漂白性,氯气和水反应生成盐酸和次氯酸,方程式为:Cl2+H2O?HCl+HClO,次氯酸具有漂白性,
故答案为:装置B中的有色布条不褪色,装置C中的有色布条褪色;Cl2+H2O?HCl+HClO;
③实验室用氢氧化钠溶液吸收多余的Cl2,生成氯化钠和次氯酸钠,所以离子反应为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
④氯气与石灰乳反应生成氯化钙和次氯酸钙,反应的方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,同时生成碳酸钙沉淀,反应的化学方程式为:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO.
点评 本题考查氯气的制备实验,题目综合性较强,侧重分析能力及实验能力及所学知识分析问题、解决问题的能力的综合考查,注意氯气的漂白性的探究实验原理,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 它与水反应的离子方程式为NH4++H-+H2O=NH3•H2O+H2↑ | |
| B. | NH5中既有共价键又有离子键 | |
| C. | NH5的电子式为 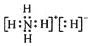 | |
| D. | 1 mol NH5中含有5 NA个N-H键(NA表示阿伏加德罗常数) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 实验装置 | 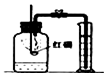 测定空气中氧气含量 | 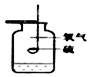 硫在氧气中燃烧 | 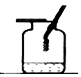 铁丝在氧气中燃烧 | 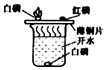 探究燃烧的条件 |
| 解释 | 量筒中水:通过水体积的变化得出O2的体积 | 集气瓶中的水:吸收放出的热量 | 集气瓶中的水:冷却溅落熔融物,防止集气瓶炸裂 | 烧杯中的水:加热铜片;隔绝空气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 醋酸 | 碳酸 | 氨水 | 氯水 |
| B | 纯碱 | 碘酒 | 苛性钾 | 醋酸 | 干冰 |
| C | 石油 | 石灰石 | 硫酸 | 磷酸 | 水 |
| D | 烧碱 | 天然气 | 氯化钠 | 碳酸钠 | 蔗糖 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡溶液与硫酸的反应:OH-+H+═H2O | |
| B. | 向澄清的石灰水中通入过量的CO2:OH-+CO2═HCO3- | |
| C. | 碳酸钙与醋酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 金属钠与硫酸铜反应:2Na+Cu2+═2Na++Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称量10.6 g Na2CO3溶于100 mL水中 | |
| B. | 称量10.6 g Na2CO3•10H2O溶于少量水中,再用水稀释至100 mL | |
| C. | 量取20 mL 5.0 mol/L Na2CO3溶液用水稀释至100 mL | |
| D. | 配制80 mL 1.0 mol/L Na2CO3溶液,则只需要称量8.5 g Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述I | 陈述II |
| A | Fe2O3是红棕色粉末 | Fe2O3常做红色涂料 |
| B | SiO2是两性氧化物 | SiO2可和HF反应 |
| C | Al2O3难溶于水 | Al2O3可用作耐火材料 |
| D | SO2有漂白性 | SO2可使溴水褪色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气的燃烧热△H=-241.6 kJ•mol-1 | |
| B. | 等质量的H2、CO完全燃烧时,CO释放的热量更多 | |
| C. | 煤的气化的热化学方程式为C(s)+H2O(g)═CO(g)+H2(g)△H=-131.1 kJ•mol-1 | |
| D. | 煤炭完全燃烧释放1967.5 kJ热量时转移20 mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com