������ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W��X
-������Li
+������ͬ�ĵ��Ӳ�ṹ����XΪHԪ�أ���Ԫ�����ڱ��У�Y��Z���ڣ�Z��W���ڣ���Y������������Ϊa������Ԫ��ͬ�������ڣ���Z��W�������������ֱ�Ϊa+1��a+2����1+a+a+1+a+2=18�����a=
�����������⣻��Y��Zͬ���壬Z��Wͬ���ڣ���W����������Ϊa+1����1+a+a+a+1=18�����a=
�����������⣻��Y��Zͬ���ڣ�Z��Wͬ���壬��Z��W����������Ϊa+1����1+a+a+1+a+1=18�����a=5����YΪNԪ�ء�ZΪOԪ�ء�WΪSԪ�أ�
��1�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС��
��2����H��N��O����Ԫ����ɵĻ�����A�мȺ������Ӽ����ֺ��й��ۼ���Ϊ����炙�������泥�
��3����B��C������H��N��O��S����Ԫ�ع�ͬ��ɵ����ӻ����1molB������NaOHŨ��Һ��Ӧ�����ɱ�״����44.8L���壨������������ʧ����������Ϊ�����������ʵ���=
=2mol��B��C��ˮ��Һ�з�Ӧ������ų�����BΪ��NH
4��
2SO
3��CΪNH
4HSO
4��
��4������O��S��Ԫ�غ���һ��Ԫ��Q�����һ������D��������D����Һ����NaOH��Һ��������ɫ�������ð�ɫ�������ɺ�Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ����D��Һ�к���Fe
2+����ȡ����D��Һ���������BaCl
2��Һʱ������ɫ�������Ҽ���������ʱ�������ܽ⣬��D��Һ�к���SO
42-����DΪFeSO
4�����ݵ���ת���غ����MnԪ���ڻ�ԭ�����еĻ��ϼۣ��жϻ��в����ƽ��д���ӷ���ʽ��
����⣺ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W��X
-������Li
+������ͬ�ĵ��Ӳ�ṹ����XΪHԪ�أ���Ԫ�����ڱ��У�Y��Z���ڣ�Z��W���ڣ���Y������������Ϊa������Ԫ��ͬ�������ڣ���Z��W�������������ֱ�Ϊa+1��a+2����1+a+a+1+a+2=18�����a=
�����������⣻��Y��Zͬ���壬Z��Wͬ���ڣ���W����������Ϊa+1����1+a+a+a+1=18�����a=
�����������⣻��Y��Zͬ���ڣ�Z��Wͬ���壬��Z��W����������Ϊa+1����1+a+a+1+a+1=18�����a=5����YΪNԪ�ء�ZΪOԪ�ء�WΪSԪ�أ�
��1��H
-��Li
+���ӵ��Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶H
-��Li
+��
�ʴ�Ϊ������
��2����H��N��O����Ԫ����ɵĻ�����A�мȺ������Ӽ����ֺ��й��ۼ�������A�Ļ�ѧʽΪNH
4NO
3�ȣ�
�ʴ�Ϊ��NH
4NO
3�ȣ�
��3��B��C������H��N��O��S����Ԫ�ع�ͬ��ɵ����ӻ����1molB������NaOHŨ��Һ��Ӧ�����ɱ�״����44.8L���壨������������ʧ����������Ϊ�����������ʵ���=
=2mol��B��C��ˮ��Һ�з�Ӧ������ų�����BΪ��NH
4��
2SO
3��CΪNH
4HSO
4����
�ټ���������B��NaOHŨ��Һ��Ӧ�Ļ�ѧ����ʽΪ����NH
4��
2SO
3+2NaOH
Na
2SO
3+2NH
4��
2+2H
2O��
��B��Cˮ��Һ��Ӧ�����ӷ���ʽΪ��2H
++SO
32-=SO
2��+H
2O��
�ʴ�Ϊ����NH
4��
2SO
3+2NaOH
Na
2SO
3+2NH
4��
2+2H
2O��2H
++SO
32-=SO
2��+H
2O��
��4����O��S��Ԫ�غ���һ��Ԫ��Q�����һ������D��������D����Һ����NaOH��Һ��������ɫ�������ð�ɫ�������ɺ�Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ����D��Һ�к���Fe
2+����ȡ����D��Һ���������BaCl
2��Һʱ������ɫ�������Ҽ���������ʱ�������ܽ⣬��D��Һ�к���SO
42-����
��D�Ļ�ѧʽΪFeSO
4��
��1mol?L
-1l00mLFeSO
4����Һ����1mol?L
-1 20mL KMnO
4��Һ�������ữ��ǡ�÷�Ӧ��Fe
2+������ΪFe
3+����MnԪ���ڻ�ԭ�����еĻ��ϼ�Ϊa�����ݵ���ת���غ��֪��0.1L��1mol/L����3-2��=0.02L��1mol/L����7-a�������a=2��������Mn
2+����Ӧ���ӷ���ʽΪ��5Fe
2++MnO
4-+8H
+=5Fe
3++Mn
2++4H
2O��
�ʴ�Ϊ��FeSO
4��5Fe
2++MnO
4-+8H
+=5Fe
3++Mn
2++4H
2O��
���������⿼��ṹ����λ�ù�ϵӦ�á��뾶�Ƚϡ������ƶϡ�������ԭ��Ӧ�����ӷ���ʽ�ȣ��Ѷ��еȣ��ƶ�Ԫ���ǽ���ؼ����ƶ���ע��ȷ��Y��Z��W�Ŀ���λ�ù�ϵ��Ҫ��������Ԫ�ػ��������ʣ����ض�ѧ�����������������飮



 ������ȫ�̼����ĩ���100��ϵ�д�
������ȫ�̼����ĩ���100��ϵ�д�
 H2SO3��H2SO3
H2SO3��H2SO3 H++HSO3-
H++HSO3- H2SO3��H2SO3
H2SO3��H2SO3 H++HSO3-
H++HSO3-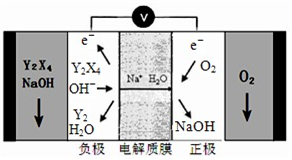
 X��Y��Z��WΪ��ԭ��������С�������е����ֶ�����Ԫ�أ���֪����X�ɷֱ���Y��W�γ�X2Y��X2Y2��XW�ȹ��ۻ������Z�ɷֱ���Y��W�γ�Z2Y��Z2Y2��ZW�����ӻ����
X��Y��Z��WΪ��ԭ��������С�������е����ֶ�����Ԫ�أ���֪����X�ɷֱ���Y��W�γ�X2Y��X2Y2��XW�ȹ��ۻ������Z�ɷֱ���Y��W�γ�Z2Y��Z2Y2��ZW�����ӻ����