
 2NH3(g)�����ڵ�ⷨ�ϳɰ��Ĺ����У�Ӧ��H2���ϵ�ͨ��_________����������������� ������һ�缫ͨ��N2���õ缫�ķ�ӦʽΪ__________________________��
2NH3(g)�����ڵ�ⷨ�ϳɰ��Ĺ����У�Ӧ��H2���ϵ�ͨ��_________����������������� ������һ�缫ͨ��N2���õ缫�ķ�ӦʽΪ__________________________�� 4NH3(g)��3O2(g) ��H��Q��
4NH3(g)��3O2(g) ��H��Q��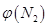 �뷴Ӧ�¶�T�Ĺ�ϵ������ͼ��ʾ����������Ӧ��Q________0�����������������=������
�뷴Ӧ�¶�T�Ĺ�ϵ������ͼ��ʾ����������Ӧ��Q________0�����������������=������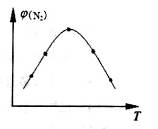
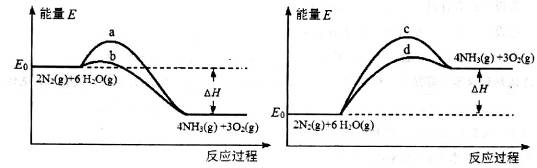
 2NH3(g) ��H����93.0kJ/mol��
2NH3(g) ��H����93.0kJ/mol��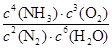 ��2�֣���2������2�֣� ��3��d��2�֣�
��2�֣���2������2�֣� ��3��d��2�֣�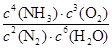 ��
�� 2NH3(g)�ͷ�Ӧ��2N2(g)��6H2O(g)
2NH3(g)�ͷ�Ӧ��2N2(g)��6H2O(g) 4NH3(g)��3O2(g)����������ݸ�˹���ɿ�֪���١�
4NH3(g)��3O2(g)����������ݸ�˹���ɿ�֪���١�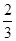 ���ڡ�
���ڡ�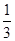 ���õ���ӦO2(g)��2H2(g)��2H2O(g)�����Ը÷�Ӧ�ķ�Ӧ�ȡ�H��2/3������93 kJ��mol��1����1/3��1530 kJ��mol��1����572 kJ��mol��1��
���õ���ӦO2(g)��2H2(g)��2H2O(g)�����Ը÷�Ӧ�ķ�Ӧ�ȡ�H��2/3������93 kJ��mol��1����1/3��1530 kJ��mol��1����572 kJ��mol��1�� 2NH3(g)��֪��4mol�ķ�Ӧ����ȫ��Ӧ�������ʵ�����С2mol����˵����٣�4��2.8��mol��1.2molʱ���μӷ�Ӧ��H2Ϊ1.8mol������������ת����Ϊ
2NH3(g)��֪��4mol�ķ�Ӧ����ȫ��Ӧ�������ʵ�����С2mol����˵����٣�4��2.8��mol��1.2molʱ���μӷ�Ӧ��H2Ϊ1.8mol������������ת����Ϊ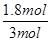 ��100%��60����
��100%��60����

 �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������п�̸ɵ�� | B��Ǧ���� |
| C������ȼ�ϵ�� | D��̫���ܵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
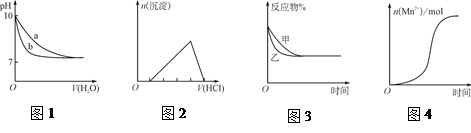
| A��ͼ1��ʾ��ͬ�¶��£���pH��10������������Һ�Ͱ�ˮ�зֱ��ˮϡ��ʱpH�ı仯���ߣ�����a��ʾ��ˮϡ��ʱpH�ı仯���� |
| B��ͼ2��ʾ���������������Ƶ�ƫ��������Һ�еμ��������ó������ʵ�������������Ĺ�ϵ |
C��ͼ3��ʾѹǿ�Կ��淴ӦCO(g)��H2O(g)  CO2(g)��H2(g)��Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ�� CO2(g)��H2(g)��Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ�� |
| D��ͼ4��ʾ10 mL 0.01 mol��L��1KMnO4������Һ�������0.1 mol��L��1 H2C2O4��Һ���ʱ��n(Mn2��)��ʱ��ı仯(Mn2���Ը÷�Ӧ�д�����) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ѧ��Ӧ���� | B����ѧ��Ӧ��ƽ�ⳣ�� |
| C��ˮ�����ӻ� | D�����ȷ�Ӧ��Ӧ���ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ͨ�����ͻ�ѧ��Ӧ���ʱ�ӿ컯ѧ��Ӧ���� |
| B��Ǧ���س��ʱ�����С�һ���ĵ缫Ӧ���Դ�ĸ������� |
| C���¶ȱ��ֲ��䣮��ˮ�м������ζ�ˮ�ĵ���һ��û��Ӱ�� |
| D�����������Һ�м�ˮϡ��ʱ����Һ����������Ũ�ȶ���С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
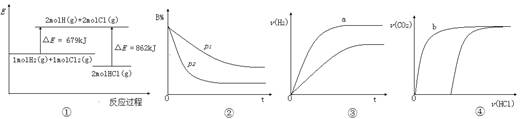
| A���ٱ�ʾ��ӦH2(g)+Cl2(g)=2HCl(g)�������仯����÷�Ӧ�ġ�H="183" kJ��mol-1 |
B���ڱ�ʾ������������ʱ����Ӧ4A(g)+3B(g) 2C(g)+6D�ڲ�ͬѹǿ��B��(B���������)��ʱ��ı仯����Dһ�������� 2C(g)+6D�ڲ�ͬѹǿ��B��(B���������)��ʱ��ı仯����Dһ�������� |
| C���۱�ʾ�����pH����ͬ��HCl��CH3COOH������Һ�У��ֱ����������п������H2�������ʱ��ı仯����a��ʾ����HCl��Һ |
| D���ܱ�ʾ10 mL 0.1 mol��L-1 Na2CO3��NaHCO3������Һ�У��ֱ�μ�0.l mol/L HCl��Һʱ��CO2���������������ı仯����b��ʾ����NaHCO3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 H2NCOONH4(���������)(l) ��H1
H2NCOONH4(���������)(l) ��H1 H2O+ H2NCONH2(l)��H2
H2O+ H2NCONH2(l)��H2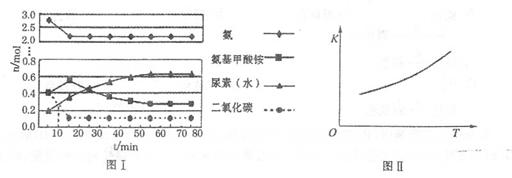
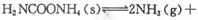
 ��ʵ���ò�ͬ�¶��µ�ƽ�����������±���
��ʵ���ò�ͬ�¶��µ�ƽ�����������±���| �¶�/�� | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| ƽ����ѹǿ/Kpa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| ƽ��������Ũ��/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
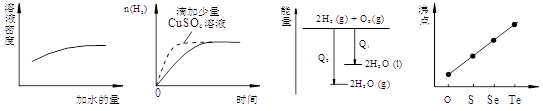
| A��ϡ�����ϡ�� | B�������������������п�۷�Ӧ | C��������������Ӧ�е������仯 | D����̬�⻯��е� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
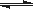 Si3N4��s��+6CO��g��
Si3N4��s��+6CO��g��| ʱ��/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 |
| N2Ũ��/mol��L-1 | 4��00 | 3��70 | 3��50 | 3��36 | 3��26 | 3��18 | 3��10 | 3��00 | 3��00 | 3��00 |
| COŨ��/mol��L-1 | 0��00 | 0��90 | 1��50 | 1��92 | 2��22 | 2��46 | 2��70 | | | |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com