



 .
. 分析 (1)氮气中存在3对共用电子对,氮原子最外层达到8个电子;
(2)氯化钾为离子化合物,钾离子与氯离子通过离子键结合;
(3)硫化钠是离子化合物,硫化钠的电子式中含有两个钠离子;
(4)CO2 中C分别为O形成2对共价键,属于共价化合物;
解答 解:(1)氮气中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气的电子式为 ;
;
故答案为: ;
;
(2)KCl存在钾离子和氯离子,钾离子为简单阳离子,氯离子最外层为8电子,氯化钾的电子式为 ,
,
故答案为: ;
;
(3)硫化钠的化学式中含有两个钠离子,硫化钠正确的电子式为: ,
,
故答案为: ;
;
(4)CO2 中C分别为O形成2对共价键,电子式为: ,
,
故答案为: .
.
点评 本题考查了电子式的书写,明确离子化合物与共价化合物的电子式的表示方法及区别是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 酸性:HClO4>H3PO4>H2SO4 | B. | 氢化物稳定性:HF>H2O>NH3 | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 氧化性:F2>O2>N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
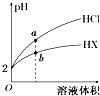 25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )
25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )| A. | a、b两点:c(X-)>c(Cl-) | B. | 稀释10倍,HX溶液的pH=3 | ||
| C. | 稀释前,c(HX)=0.01 mol•L-1 | D. | 溶液的导电性:a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三种物质质子数之比为1:2:3 | B. | 三种物质中子数之比为1:1:1 | ||
| C. | 三种物质的摩尔质量之比为8:9:10 | D. | 三种物质的化学性质不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径 (10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
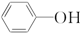 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子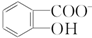 能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是
能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是 中形成分子内氢键,使其更难电离出H+;水杨酸分子中苯环和羧基上碳原子的杂化方式分别是sp2杂化和sp2杂化.
中形成分子内氢键,使其更难电离出H+;水杨酸分子中苯环和羧基上碳原子的杂化方式分别是sp2杂化和sp2杂化.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com