
��֪N2(g)+3H2(g) 2NH3(g) ��H=-92��3kJ/mol����һ���¶Ⱥʹ����������£���һ�ܱ������У�ͨ��1molN2��3molH2���ﵽƽ��״̬I����ͬ�����£�����һ�����ͬ���ܱ�������ͨ��0��9molN2��2��7molH2��0��2molNH3���ﵽƽ��״̬II��������˵����ȷ����
2NH3(g) ��H=-92��3kJ/mol����һ���¶Ⱥʹ����������£���һ�ܱ������У�ͨ��1molN2��3molH2���ﵽƽ��״̬I����ͬ�����£�����һ�����ͬ���ܱ�������ͨ��0��9molN2��2��7molH2��0��2molNH3���ﵽƽ��״̬II��������˵����ȷ����
| A������ƽ��״̬��ƽ�ⳣ���Ĺ�ϵ��K����K�� |
| B��H2�İٷֺ�����ͬ |
| C��N2��ת���ʣ�ƽ��I<ƽ��� |
| D����Ӧ�ų���������Q��=Q����92��3kJ |
B
���������������������ͬ�������н��е�ͬһ�����淴Ӧ���ڵڶ��������������Ϊ0��2molNH3���Ǽ���������ķ�Ӧ�����ɵġ���Чת����ȥ�����ݷ���ʽ��֪����0��2molNH3����N20��1mol�� H20��3mol�����൱�ڿ�ʼ����������ʵ���Ϊ1molN2��3molH20 molNH3�����������Ͷ�Ϸ�ʽ����ʼ״̬��ͬ���ﻯѧƽ��ʱ״̬Ҳ��ͬ��ƽ��ʱ����ֵĺ�����ͬ����Ӧ���ת���ʵȵ�Ҳ��һ��������A��C��D����B��ȷ��
���㣺�����Чƽ�������֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����һ�����ܱ������У���������A��B��C��������һ�������·�����Ӧ���������»�ѧƽ�⣺aA(g) + bB(g) xC(g)��������ͼ��ʾ�Ĺ�ϵ��c%��ʾƽ�������в���C�İٷֺ�����T��ʾ�¶ȣ�p��ʾѹǿ������ͼ�У�Y����ָ
xC(g)��������ͼ��ʾ�Ĺ�ϵ��c%��ʾƽ�������в���C�İٷֺ�����T��ʾ�¶ȣ�p��ʾѹǿ������ͼ�У�Y����ָ
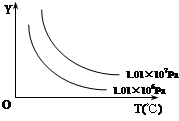
A����Ӧ��A�İٷֺ��� B����Ӧ��B��ƽ��ת����
C��ƽ���������ܶ� D��ƽ�������������ʵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����ܱ������еķ�Ӧ��2SO2(g)+O2(g) 2SO3(g) ��H<0��450��ʱ��n(SO3)��n(O2)��ʱ��ı仯��ϵ��ͼ��ʾ������˵����ȷ����
2SO3(g) ��H<0��450��ʱ��n(SO3)��n(O2)��ʱ��ı仯��ϵ��ͼ��ʾ������˵����ȷ����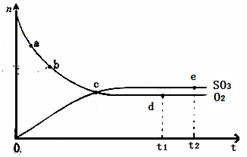
| A����c����Ӧ�ﵽƽ�� |
| B����a������Ӧ���ʱȵ�b�Ĵ� |
| C����d (t1ʱ��)�͵�e (t2ʱ��)��n(SO2)��һ�� |
| D�������������䣬600��ʱ��Ӧ��t1ʱ�̣�n(SO 3)����ͼ�е�d��ֵҪ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ij��Ӧ2A(g) A(g)+2B(g)����֪��H<0�������ж���ȷ����
A(g)+2B(g)����֪��H<0�������ж���ȷ����
| A���������·�Ӧ�����Է����� | B���������·�Ӧ�����Է����� |
| C���κ��¶��·�Ӧ�������Է����� | D���κ��¶��·�Ӧ�������Է����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������ʵ�У���������������ԭ�����͵���
| A��Fe(SCN)3����Һ�м������KSCN����ɫ���� |
| B����ϡ�����м�����������ˮ��������������Ũ�Ƚ��� |
| C��ʵ���ҳ����ű���ʳ��ˮ�ķ����ռ����� |
| D���غ�ɫNO2����ѹ����ɫ�ȱ�����dz |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ҵ�ϲ�����ϩ��ˮ�����ڴ���������/������������ϳ��Ҵ�����Ӧԭ��Ϊ��
CH2��CH2��g��+H2O��g�� CH3CH2OH��g����H ��0���ﵽƽ��ʱ��Ҫʹ��Ӧ���ʼӿ죬ͬʱ��ϩ��ת������ߣ�Ӧ��ȡ�Ĵ�ʩ��
CH3CH2OH��g����H ��0���ﵽƽ��ʱ��Ҫʹ��Ӧ���ʼӿ죬ͬʱ��ϩ��ת������ߣ�Ӧ��ȡ�Ĵ�ʩ��
| A�����뺤�� | B��������Ҵ� | C������ѹǿ | D�������¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���и��鷴Ӧ(�������ʾ�Ϊ��Ӧ��)����Ӧ�տ�ʼʱ���ų�H2������������
| ��� | ����(��ĩ״) /mol | ���Ũ������� | ��Ӧ�¶� |
| A | Mg 0.1 | 6mol/L HNO3 10 mL | 60 �� |
| B | Mg 0.1 | 3mol/L HCl 10 mL | 60 �� |
| C | Fe 0.1 | 3mol/L HCl 10 mL | 60 �� |
| D | Mg 0.1 | 3mol/L H2SO4 10 mL | 60 �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ�������Ļ���������ܱ������з������·�Ӧ��xA(g)+yB(g) zC(g)���ﵽƽ����A�����Ũ��Ϊ0.5mol/L���������½��ܱ��������ݻ�����ԭ���Ķ������ٴ�ƽ����A��Ũ��Ϊ0.3mol/L������������ȷ����
zC(g)���ﵽƽ����A�����Ũ��Ϊ0.5mol/L���������½��ܱ��������ݻ�����ԭ���Ķ������ٴ�ƽ����A��Ũ��Ϊ0.3mol/L������������ȷ����
| A��ƽ��������Ӧ�����ƶ� | B��x+y��z |
| C��C������������� | D��B��ת�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������ʵ����ʵ����������Ӧ������ȷ���� �� ��
| ѡ�� | ʵ����ʵ | ���� |
| A | ����������ͬ��Na2S2O3��ҺŨ��Խ���������������ʱ��Խ�� | ��������������ʱ������Ӧ��Ũ�Ȼ�ѧ��Ӧ���ʼӿ� |
| B | �ڻ�ѧ��Ӧǰ�����������ͻ�ѧ���ʶ�û�з����ı� | ����һ�������뻯ѧ��Ӧ |
| C | ���ʵ���Ũ����ͬ������ʹ���ֱ������������״��ͬ��п����Ӧ | ��Ӧ��ʼ������ͬ |
| D | ���ݻ��ɱ���ܱ������з�����Ӧ H2(g)+I2(g)  2HI(g)�����ݻ���Сһ�� 2HI(g)�����ݻ���Сһ�� | ����Ӧ���ʼӿ죬�淴Ӧ���ʲ��� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com