
【题目】电解CuSO4溶液时,若要达到如下三个要求:①阳极质量减小;②阴极质量增加;③电解质溶液中Cu2+浓度不变。则选用的电极是( )
A.纯铜作阳极,含锌、银的铜合金作阴极
B.铁作阳极,铜作阴极
C.石墨作阳极,铂作阴极
D.含锌、银的铜合金作阳极,纯铜作阴极
科目:高中化学 来源: 题型:
【题目】下列去除杂质(括号内的物质为杂质)的方法中,不正确的是
A. NaCl固体(I2):充分加热
B. Fe粉(Al):加入足量NaOH溶液,溶解后过滤
C. SiO2固体(CaO):加入足量稀HCl,溶解后过滤
D. CO2气体(HCl):通入饱和Na2CO3溶液,洗气后干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 锌与CH3COOH溶液反应:Zn+2H+===Zn2++H2↑
B. 氢氧化铝与稀硝酸反应:H++OH-===H2O
C. CuCl2溶液与铁粉反应:3Cu2++2Fe===3Cu+2Fe3+
D. MgCl2溶液与氨水反应:Mg2++2NH3·H2O===Mg(OH)2↓+2NH![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. H2O的沸点比H2S高,所以H2O比H2S更稳定
B. 干冰和石英晶体中的化学键类型相同,熔化时需克服微粒间的作用力类型也相同
C. N2和CCl4中,每个原子的最外层都具有8电子稳定结构
D. NaHCO3受热分解的过程中,只有离子键被破坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某微粒用AZRn+表示,下列关于该微粒的叙述正确的是( )
A. 所含质子数=A-n B. 所含中子数=A-Z
C. 所含电子数=Z+n D. 质量数=Z+A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碲(Te)广泛用于彩色玻璃和陶瓷。工业上用精炼铜的阳极泥(含有质量分数为8%的TeO2、少量Ag、Au)为原料制备单质碲的一种工艺流程如下:(已知TeO2微溶于水,易溶于强酸和强碱)
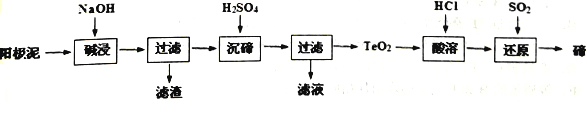
下列有关说法不正确的是
A. 将阳极泥研磨、反应适当加热都有利于提高“碱浸”的速率和效率
B. “沉碲”时为使碲元素沉淀充分,应加入过量的硫酸
C. “碱浸”时发生主要反应的离子方程式为TeO2+2OH-=TeO32-+H2O
D. 若提取过程碲元素的回收率为90%,则处理IKg这种阳极泥最少需通入标准状况下SO220.16L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是( )。
A.海水中含有钾元素,只需经过物理变化就可以得到钾单质
B.海水蒸发制海盐的过程中只发生了化学变化
C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2
D.利用潮汐发电是将化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~D是四种烃分子的球棍模型(如图). 
(1)与A互为同系物的是(填序号).
(2)能使酸性高锰酸钾溶液褪色的物质是(填序号).
(3)C的同分异构体的结构简式是 .
(4)D和液溴反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y 各0.16 mol充入10 L 恒容密闭容器中,发生反应:X(g)+ Y(g)![]() 2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表。下列说法正确的是 ( )
2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表。下列说法正确的是 ( )
t / min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. 反应前2min的平均速率v(Z)=2.0×10-5 mol/(L·min)
B. 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C. 该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2 mol Z,平衡时X的物质的量浓度减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com