
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案科目:高中化学 来源: 题型:解答题
| 步骤 | 操作 | 现象及结论 |
| 1 | 用甲、乙两支试管分别取两种溶液各少许. | |
| 2 | 用胶头滴管向甲试管中逐滴滴加BaCl2溶液至过量. | |
| 3 | 静置,将甲中上层清液注入乙中 | 若产生白色沉淀,则甲是Na2SO3溶液,乙是稀H2SO4. 若乙试管中沉淀溶解且放出有刺激性气味的气体,则甲是稀H2SO4,乙是Na2SO3溶液. |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | H2S?2H++S2- | B. | KHSO4?K++H++SO42- | ||
| C. | Al(OH)3?Al3++3OH- | D. | NaH2PO4═Na++H2PO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 实验 | 制取蒸馏水 | 制取NH3 | 收集NO2 | 分离水和酒精 |
| 装置 或 仪器 | 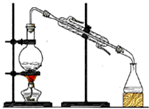 |  |  | 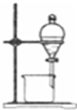 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
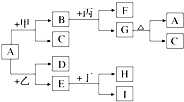 如图是有关物质相互转化的关系图,其中A俗称铁红,甲为强酸,乙、H为还原性气体,丁为一种常见的挥发性酸,G为红褐色沉淀,I的颜色呈浅绿色.
如图是有关物质相互转化的关系图,其中A俗称铁红,甲为强酸,乙、H为还原性气体,丁为一种常见的挥发性酸,G为红褐色沉淀,I的颜色呈浅绿色.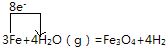 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用蒸馏可以除去水等液体中难挥发或不挥发的杂质 | |
| B. | 酒精是一种常用萃取剂,若用来萃取溴水中的溴,由于密度小静置后在上层 | |
| C. | 混有少量氯化钾的硝酸钾,可以利用过滤的方法得到纯净的硝酸钾晶体 | |
| D. | 用分液漏斗将溴水中的下层液溴放出的方法为分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:2 | B. | 2:3 | C. | 3:1 | D. | 1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 操作及现象 | 结论 |
| A | 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4溶液颜色基本不变 | Fe(NO3)2与H2SO4不反应 |
| B | 常温下,测得饱和Na2CO3溶液的pH大于饱和NaHCO3溶液 | 常温下水解程度: CO32->HCO3- |
| C | 向25mL冷水和沸水中分别滴入5滴FeCl3饱和溶液,前者为黄色,后者为红褐色 | 温度升高,Fe3+的水解程度增大 |
| D | 滴加几滴稀NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝 | 原溶液中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=3 | B. | C(OH-)=10-8mol/l | C. | pH=11 | D. | C(H+)=10-4mol/l |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com