
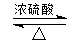
 CH3COOCH2CH3+H2O.反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是NaOH溶液.
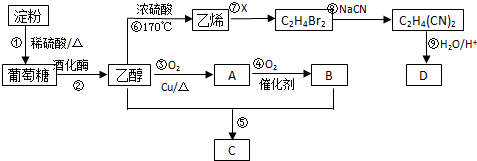
CH3COOCH2CH3+H2O.反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是NaOH溶液.分析 CH3CH2OH在Cu催化剂条件下发生催化氧化生成A为CH3CHO,CH3CHO进一步氧化生成B为CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成C为CH3COOC2H5,乙醇发生消去反应生成乙烯,乙烯与Br2发生加成反应生成BrCH2CH2Br,BrCH2CH2Br与NaCN发生取代反应生成NC-CH2CH2-CN,(4)中D的相对分子量为118,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则分子中N(C)=$\frac{118×40.68%}{12}$=4、N(H)=$\frac{118×5.08%}{1}$=6、N(O)=$\frac{118-12×4-6}{16}$=4,故D的分子式为C4H6O4,则其结构简式为HOOC-CH2CH2-COOH.
解答 解:CH3CH2OH在Cu催化剂条件下发生催化氧化生成A为CH3CHO,CH3CHO进一步氧化生成B为CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成C为CH3COOC2H5,乙醇发生消去反应生成乙烯,乙烯与Br2发生加成反应生成BrCH2CH2Br,BrCH2CH2Br与NaCN发生取代反应生成NC-CH2CH2-CN,(4)中D的相对分子量为118,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则分子中N(C)=$\frac{118×40.68%}{12}$=4、N(H)=$\frac{118×5.08%}{1}$=6、N(O)=$\frac{118-12×4-6}{16}$=4,故D的分子式为C4H6O4,则其结构简式为HOOC-CH2CH2-COOH.
(1)A的结构简式为CH3CHO,反应②葡萄糖在催化剂作用下发生反应生成乙醇,反应的化学方程式为C6H12O6$\stackrel{酒化酶}{→}$2CH3CH2OH+2CO2,
故答案为:CH3CHO;C6H12O6$\stackrel{酒化酶}{→}$2CH3CH2OH+2CO2;
(2)反应⑦中物质X的分子式为Br2,反应⑧的类型为取代反应,
故答案为:Br2;取代反应;
(3)反应⑤的化学方程式为CH3COOH+CH3CH2OH
故答案为:CH3COOH+CH3CH2OH 
(4)由上述分析可知,D的分子式为:C4H6O4,
故答案为:C4H6O4;
(5)反应①是淀粉水解生成葡萄糖,葡萄糖中含有醛基,检验否发生的实验方案:取反应①的溶液2mL于试管中,用10%的NaOH溶液调节溶液至中性,再向其中加入2 mL 10%的NaOH溶液,再加入4~5滴5%的CuSO4溶液,加热一段时间.若有砖红色沉淀,则证明反应①已发生,
故答案为:用10%的NaOH溶液调节溶液至中性,再向其中加入2 mL 10%的NaOH溶液,再加入4~5滴5%的CuSO4溶液,加热一段时间.若有砖红色沉淀,则证明反应①已发生.
点评 本题考查有机物的推断与合成,侧重考查学生分析推理能力、知识迁移运用能力,熟练掌握官能团的性质与转化,注意常见有机物与官能团的检验.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题

| A. | 装置①常用于分离互不相溶的液体 | B. | 装置②可用于吸收NH3 | ||
| C. | 装置③可用于收集NO、CO2等气体 | D. | 装置④可用于制备乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ①③④ | C. | ②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c的原子半径是这些元素中最大的 | |
| B. | b与其他三种元素均可形成至少两种二元化合物 | |
| C. | a与其他三种元素形成的二元化合物中其化合价均为+1 | |
| D. | d和a形成的化合物的溶液呈弱酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
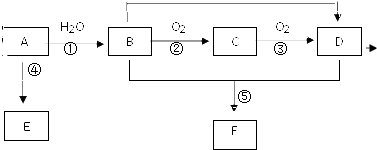 已知 A 的产量通常用来衡量一个国家的石油化工水平,现以 A 为主要原料合成高分子化合物 E 和一种具有果香味的物质 F,其合成路线如图所示.
已知 A 的产量通常用来衡量一个国家的石油化工水平,现以 A 为主要原料合成高分子化合物 E 和一种具有果香味的物质 F,其合成路线如图所示.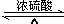 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
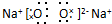 ,甲中的化学键类型为离子键、共价键.
,甲中的化学键类型为离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
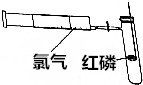 已知SnCl4、SiCl4、AlCl3、PCl3、PCl5等氯化物在潮湿的空气中都有白雾生成.为清楚地观察磷在氯气中燃烧,达到PCl3和PCl5分步生成的目的,可预先把干燥的氯气贮存在100mL的注射器内,再把火柴头大小的红磷置于玻璃燃烧匙上烘干后组成如图所示的装置.
已知SnCl4、SiCl4、AlCl3、PCl3、PCl5等氯化物在潮湿的空气中都有白雾生成.为清楚地观察磷在氯气中燃烧,达到PCl3和PCl5分步生成的目的,可预先把干燥的氯气贮存在100mL的注射器内,再把火柴头大小的红磷置于玻璃燃烧匙上烘干后组成如图所示的装置.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com