
| A. | 用碳棒连接电源的正极,另一电极用铜片 | |
| B. | 用铜片连接电源的正极,另一电极用铂片 | |
| C. | 阳极反应式为:Cu-2e═Cu2 | |
| D. | 阴极反应式为:2H++2e═H2↑ |
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某研究小组取一定质量的镁铝合金材料投入200mL稀硫酸中,待固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示.请回答下列问题
某研究小组取一定质量的镁铝合金材料投入200mL稀硫酸中,待固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示.请回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 A.B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去).
A.B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 恒温时压强不再改变的状态 | |
| B. | 体系温度不在改变的状态 | |
| C. | 恒温时混合气体的密度不再改变的状态 | |
| D. | 混合气体的平均相对分子质量不再改变的状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
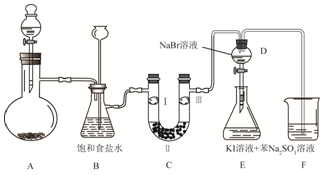
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 工业合成氮属于人工固氮 | |
| B. | 含氮无机物和含氮有机物可以相互转化 | |
| C. | 氮的固定不一定是化学变化 | |
| D. | 碳、氢、氧三种元素也参与了氮循环 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 室温下,将1.000mol•L-1盐酸滴入20.00mL 1.000mol•L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法不正确的是( )
室温下,将1.000mol•L-1盐酸滴入20.00mL 1.000mol•L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法不正确的是( )| A. | a点:由水电离出的c(H+)>1.0×10-14mol•L-1 | |
| B. | b点:c(NH4+)+c(NH3•H2O)>c(Cl-) | |
| C. | c点:c(Cl-)>c(NH4+) | |
| D. | d点后,溶液温度略下降的主要原因不可能是NH3•H2O电离吸热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com