
| A. | 铵盐都易溶于水 | |
| B. | 由于易溶,Na+、K+、NH4+都不可能在相关离子方程式中出现 | |
| C. | NH4Cl的分解与NH3、HCl的化合不属于可逆反应 | |
| D. | 铵盐都能与NaOH反应 |
分析 A.铵盐都是可溶性的强电解质;
B.铵根离子能参加离子反应,所以能在离子方程式中出现;
C.在相同条件下,既能向正反应方向进行同时又能向逆反应方向进行的反应是可逆反应;
D.铵盐都能和碱反应生成一水合氨.
解答 解:A.铵盐都是可溶性的强电解质,所以铵盐都易溶于水,故A正确;
B.铵根离子能参加离子反应,所以能在离子方程式中出现,如NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O,故B错误;
C.氯化铵受热易分解生成NH3、HCl,NH3、HCl相遇立即反应生成NH4Cl,反应条件不同,所以不是可逆反应,故C正确;
D.铵根离子和氢氧根离子反应生成弱电解质一水合氨,符合复分解反应条件,所以铵盐都能与NaOH反应,故D正确;
故选B.
点评 本题考查铵盐性质,铵盐都是可溶性强电解质,都能和碱反应,侧重考查复分解反应条件及基本概念,易错选项是B.


科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +319.68kJ•mol-1 | B. | +259.7kJ•mol-1 | C. | -319.68kJ•mol-1 | D. | -259.7kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将某气体点燃,产生淡蓝色火焰,该气体一定是H2S | |
| B. | 将某气体通入紫色石蕊中,溶液变红,该气体一定是CO2 | |
| C. | 向某溶液中加入硝酸酸化的氯化钡溶液,生成白色沉淀,溶液中一定含有SO42- | |
| D. | 向某溶液中加入适量浓氢氧化钠溶液共热,产生气体能使湿润红色石蕊试纸变蓝,溶液中一定含有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
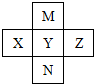
| A. | M形成的氢化物有2种 | |
| B. | M、Y、N的气态氢化物稳定性依次减弱 | |
| C. | X、Y、Z的含氧酸酸性依次增强 | |
| D. | Y的一种氧化物是大气污染物,是形成酸雨的主要物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
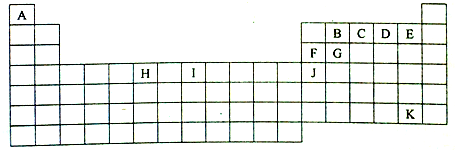
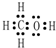 ,Y的中心原子杂化方式为SP2.
,Y的中心原子杂化方式为SP2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com