
| A. | 3 mol | B. | 2.4mol | C. | 2.2mol | D. | 3.2mol/L |
分析 利用速率之比等于其化学计量数之比计算v(B),再根据△c(B)=v(B)•△t计算B的浓度变化量△c(B),根据n=cV计算△n(B),进而计算10s时B的物质的量.
解答 解:A的平均反应速率为0.12mol•L-1•s-1,则v(B)=$\frac{1}{3}$×0.15mol•L-1•s-1=0.05mol•L-1•s-1,
故△c(B)=0.05mol•L-1•s-1×10s=0.5 mol/L,
10s后容器中B的物质的量=4mol-0.5mol•L-1×2L=3 mol,
故选A.
点评 本题考查化学反应速率的有关计算,比较基础,注意公式的理解与灵活运用,掌握基础是解题关键.


科目:高中化学 来源: 题型:选择题
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
| A. | 0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L•min) | |
| B. | 6~10的平均反应速率:v(H2O2)<3.3×10-2mol/(L•min) | |
| C. | 反应至6min时,c(H2O2)=0.20mol/L | |
| D. | 反应至6min时,H2O2分解了40% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水;无水氯化钙 | B. | 饱和NaHCO3溶;浓硫酸 | ||
| C. | 浓硫酸;饱和Na2CO3溶液 | D. | 饱和Na2CO3溶液;稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下pH=4的溶液中,Na+、SiO32-、SO42-、K+可以大量共存 | |
| B. | 对滴有酚酞的碳酸钠溶液微热,溶液颜色加深 | |
| C. | 乙醇和乙酸都能溶于水,都是电解质 | |
| D. | 室温下,某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 71gCl2中含氯原子数为2NA | |
| B. | 1molO3中含原子数为2NA | |
| C. | 1mol/L K2SO4溶液中含K+数为NA | |
| D. | 标准状况下,22.4LH2O中含水分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
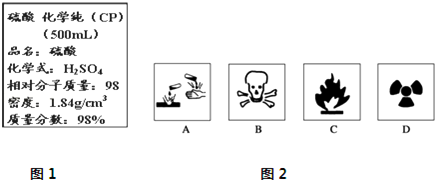
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com