
【题目】电解精炼铜时,纯铜做( ),粗铜做( )
A. 阳极 阳极 B. 阴极 阴极 C. 阳极 阴极 D. 阴极 阳极
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】下列为元素周期表中的一部分:
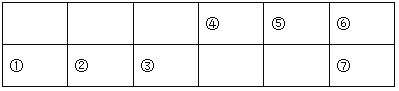
已知:⑤的氢化物常温下为气体,该气体可使湿润的红色石蕊试纸变蓝。
用化学式或元素符号回答下列问题:
(1) ④在周期表中的位置_______。
(2) ①②③中,最高价氧化物对应的水化物碱性最强的物质的电子式为_________。
(3) ①②⑥的简单离子半径由大到小的顺序是___________。(填离子符号)
(4) 用一个化学方程式证明Cl元素与⑦非金属性的强弱:____________。
(5) ①和⑥形成的一种化合物A中含有一种10电子微粒和一种18电子微粒,则A中含有的化学键类型为______。
(6) ⑥、⑦分别形成的氢化物沸点高的是_______(填化学式)。原因是_______。
(7) ①、③分别形成的最高价氧化物对应的水化物相互反应的离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以某含铜矿石[主要成分为FeCu4SiO5(OH)4,含少量SiO2、CuCO3]为原料,制备CuSO4·5H2O的流程如下:
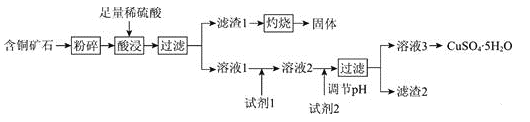
已知:
ⅰ.溶液中离子浓度小于等于1.0×10-5mol·L-1时,认为该离子沉淀完全。
ⅱ.相关试剂成分和价格如表1所示。
ⅲ.25℃时,该流程中金属离子生成氢氧化物时,开始沉淀和沉淀完全的pH如表2所示。
表1
试剂 | 成分 | 价格/(元·吨-1) |
漂白液 | 含25.2%NaClO | 450 |
双氧水 | 含30%H2O2 | 2400 |
浓硝酸 | 含98%HNO3 | 1500 |
表2
氢氧化物 | 开始沉淀的pH | 沉淀完全的pH |
Fe(OH)2 | 7.6 | 9.6 |
Fe(OH)3 | 2.7 | 3.7 |
Cu(OH)2 | 4.0 | 6.5 |
请回答:
(1)FeCu4SiO5(OH)4用氧化物的形式可表示为________。
(2)结合题中信息,所选用的试剂1的名称为________;加入该试剂时,所发生反应的离子方程式为________。
(3)加入试剂2,需调节溶液的pH的合理范围为________。试剂2可以选择下列物质中的________(填字母)。
A.Cu B.CuO
C.Cu(OH)2 D.Fe
(4)25℃时,Cu(OH)2的溶度积常数Ksp[Cu(OH)2]=________。
(5)CuSO4·5H2O溶液可用于电解精炼铜。电解精炼铜时,导线中通过9.632×104C的电量时,理论上阴极质量增加________g。(已知:1个电子的电量为1.6×10-19C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息,回答下列问题:
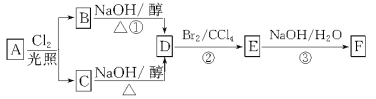
A在氧气中充分燃烧可以产生88 g CO2和45 g H2O。A的分子式是_______。
(2)B和C均为一氯代烃,它们的名称(系统命名)分别为_________________。
(3)D的结构简式________________,D中碳原子是否都处于同一平面?________。
(4)E的同分异构体的结构简式是___________________________。
(5)①、②、③的反应类型依次是_________________________。
(6)写出②、③的反应化学方程式_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,气体仅被还原的是
A. 二氧化碳使Na2O2固体变白 B. 氯气使KBr溶液变黄
C. 二氧化氮溶于水 D. 氨气使AlCl3溶液产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质按混合物、电解质、非电解质的顺序排列的是
A.盐酸、氢氧化钠醋酸、干冰
B.澄清的石灰水、铜、氨气
C.石油、水、硫酸钡
D.海水、氯化钠、氧气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com