
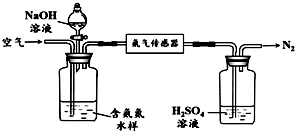
 醋酸亚铬水合物{[Cr(CH3COO2)]2•2H2O,深红色晶体}易被氧气氧化,是一种氧气吸收剂,通常以二聚体分子的形式存在,不溶于水,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示.
醋酸亚铬水合物{[Cr(CH3COO2)]2•2H2O,深红色晶体}易被氧气氧化,是一种氧气吸收剂,通常以二聚体分子的形式存在,不溶于水,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示.分析 (1)仪器1的名称为分液漏斗,使用前必须检验气密性;
(2)根据本实验的原理可知,先用锌与盐酸反应生成氢气排除装置中的空气,再利用氢气把压入醋酸钠溶液中生成醋酸亚铬水合物,据此判断,装置M是保持装置压强平衡,同时避免空气进入;
(3)配制用的蒸馏水都需事先煮沸,防止氧气氧化Cr2+;
(4)过量的锌与CrCl3充分反应得到CrCl2,实验开始生成H2气后,为使生成的CrCl2溶液与CH3COONa溶液顺利混合,打开A关闭B,把生成的CrCl2溶液压入装置3中反应;
(5)CrCl3为0.06mol,得到CrCl2为0.06mol,由方程式可知CH3COONa足量,根据CrCl2计算[Cr(CH3COO)2]2•2H2O 的理论产量,进而计算其产率.
解答 解:(1)仪器1的名称为分液漏斗,使用前必须检验气密性,
故答案为:分液漏斗;检漏;
(2)根据本实验的原理可知,先用锌与盐酸反应生成氢气排除装置中的空气,再利用氢气把压入醋酸钠溶液中生成醋酸亚铬水合物,所以醋酸钠溶液应放在装置3中,装置4是保持装置压强平衡,同时避免空气进入装置3;
故答案为:避免空气进入装置3;
(3)本实验中所用的溶液,配制用的蒸馏水都需事先煮沸,原因是,二价铬不稳定,极易被氧气氧化,去除水中的溶解氧,防止Cr2+被氧化;
故答案为:煮沸;
(4)锌粒要过量,其原因除了让产生的H2将CrCl2溶液压入装置3与CH3COONa溶液反应,隔绝空气,使体系保持还原性气氛,另一个作用是:过量的锌与CrCl3充分反应得到CrCl2,为使生成的CrCl2溶液与CH3COONa溶液顺利混合,打开A关闭B,把生成的CrCl2溶液压入装置3中反应;
故答案为:使锌与CrCl3充分反应得到CrCl2;隔绝空气,使体系保持还原性气氛;打开;关闭;
(5)CrCl3为$\frac{9.51g}{158.5g/mol}$=0.06mol,得到CrCl2为0.06mol,而CH3COONa为1.5mol,由方程式2Cr2+(aq)+4CH3COO-(aq)+2H2O(l)═[Cr(CH3COO)2]2•2H2O(s)可知CH3COONa足量,则得到[Cr(CH3COO)2]2•2H2O为0.06mol×$\frac{1}{2}$×376g/mol=11.28g,
所得产品的产率为:$\frac{8.46g}{11.28g}$×100%=75%,
故答案为:75%.
点评 本题考查物质制备实验方案的设计,题目难度中等,涉及化学仪器识别、对操作的分析评价、产率计算有关计算、对信息的获取与运用等,注意对题目信息的应用,有利于培养学生分析、理解能力及化学实验能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl、SO3的水溶液均能导电,所以NaCl、SO3均为电解质 | |
| B. | 金属元素的原子只有还原性,其阳离子只有氧化性 | |
| C. | 用激光笔照射FeCl3溶液和Fe(OH)3胶体时,产生的现象不同 | |
| D. | 合金的硬度一般小于它的成分金属,熔点高于它的成分金属 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com