
【题目】乙酸乙酯广泛用于药物、染料、香料等工业,某学习小组设计以下两套装置用乙醇、乙酸和浓硫酸分别制备乙酸乙酯(沸点77.2℃)。下列说法不正确的是

A. 浓硫酸能加快酯化反应速率 B. 不断蒸出酯,会降低其产率
C. 装置b比装置a原料损失的少 D. 可用分液的方法分离出乙酸乙酯
【答案】B
【解析】A.制取乙酸乙酯时,需要加入浓硫酸做催化剂和吸水剂;B.可逆反应,减少生成物浓度,有利于反应正向移动;C.装置b采用水浴受热均匀,比装置a原料损失的少;D.分离互不相溶的液体,可用分液的方法分离,乙酸乙酯不溶于饱和碳酸钠溶液,可用分液操作方法分离出乙酸乙酯和饱和碳酸钠溶液。
乙酸与乙醇在浓硫酸作用下加热发生酯化反应,化学反应为: CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O ,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动.故浓硫酸的作用为催化剂,吸水剂,浓硫酸能加快酯化反应速率,A正确;该制备乙酸乙酯反应为可逆反应,不断蒸出酯,减少生成物浓度,有利于反应正向移动,会提高其产率,B错误;乙醇、乙酸易挥发,甲装置则采取直接加热的方法,温度升高快,温度不易于控制,装置b采用水浴受热均匀,相对于装置a原料损失的少,C正确;分离乙酸乙酯时先将盛有混合物的试管充分振荡,让饱和碳酸钠溶液中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,静置分层后取上层得乙酸乙酯,D正确;正确选项B。
CH3COOCH2CH3+H2O ,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动.故浓硫酸的作用为催化剂,吸水剂,浓硫酸能加快酯化反应速率,A正确;该制备乙酸乙酯反应为可逆反应,不断蒸出酯,减少生成物浓度,有利于反应正向移动,会提高其产率,B错误;乙醇、乙酸易挥发,甲装置则采取直接加热的方法,温度升高快,温度不易于控制,装置b采用水浴受热均匀,相对于装置a原料损失的少,C正确;分离乙酸乙酯时先将盛有混合物的试管充分振荡,让饱和碳酸钠溶液中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,静置分层后取上层得乙酸乙酯,D正确;正确选项B。


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】过氧化钙(CaO2·8H2O)是一种在水产养殖中广泛使用的供氧剂。水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置,加入适量稀H2SO4,待MnO(OH)2与I-完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
O2![]() MnO(OH)2
MnO(OH)2![]() I2
I2![]() S4O
S4O![]()
(1)写出O2将Mn2+氧化成MnO(OH)2的离子方程式:____________________________。
(2)取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水样的溶解氧量,消耗0.010 00 mol·L-1Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧为___________ mg·L-1.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以软锰矿粉(主要含有MnO2,还含有少量的Fe2O3、Al2O3等杂质)为原料制备高纯MnO2的流程如下图所示:

已知:①常温下,Ksp[Fe(OH)3]=8.0×10-38,Ksp [Al(OH)3]=4.0×10-34。
②常温下,氢氧化物沉淀的条件:Al3+、Fe3+完全沉淀的pH分别为4.6、3.4;Mn2+开始沉淀的pH为8.1。
③常温下,当溶液中金属离子物质的量浓度小于或等于1×10-5mol·L-l时,可视为该金属离子已被沉淀完全。
(1) “酸浸”时加入一定量的硫酸,硫酸不能过多或过少。“硫酸”过多造成氨的损失;硫酸过少时,“酸浸”时会有红褐色渣出现,原因是________________________。
(2)加入氨水应调节pH的范围为__________________,当Fe3+恰好沉淀完全时,c(Al3+)=_____________mol·L-l。
(3)“过滤”所得滤渣为MnCO3,滤液中溶质的主要成分是____________(填化学式),写出其阳离子的电子式:_______________________________。
(4)加入碳酸氢铵产生沉淀的过程称为“沉锰”。
①“沉锰”过程中放出CO2,反应的离子方程式为_______________________________。
②“沉锰”过程中沉锰速率与温度的关系如图所示。当温度高于60℃时,沉锰速率随着温度升高而减慢的原因可能是________________________________________________。

(5)工业上采用间接氧化还原滴定法测定MnO2纯度,其操作过程如下:准确称量0.9200g该样品,与足量酸性KI溶液充分反应后,配制成100mL溶液。取其中20.00mL,恰好与25.00mL 0.0800mol·L-1 Na2S2O3溶液反应(I2+2S2O32-=2I-+S4O62-)。计算可得该样品纯度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列“试剂”和“试管中的物质”不能完成“实验目的”的是

实验目的 | 试剂 | 试管中的物质 | |
A | 羟基对苯环的活性有影响 | 饱和溴水 | ①苯②苯酚溶液 |
B | 甲基对苯环活性有影响 | 酸性KMnO4溶液 | ①苯②甲苯 |
C | 苯分子中没有碳碳双键 | Br2的CCl4溶液 | ①苯②己烯 |
D | 碳酸的酸性比苯酚强 | 石蕊溶液 | ①苯酚溶液②碳酸溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿酸是合成青蒿素的原料,可以由香草醛合成:

下列有关叙述正确的是
A. 香草醛的分子式是C8H10O3
B. 香草醛能与NaHCO3溶液反应
C. 两种物质均可与溴的四氯化碳溶液发生加成反应
D. 可用FeCl3溶液检验青蒿酸中是否含香草醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】严重的雾霾天气的形成与汽车尾气排放有关。汽车尾气中常含有CO、NOx等气体,为减轻污染,一般汽车都加装了“催化净化器”,可将汽车尾气中的有毒气体转化为无污染的气体。某化学兴趣小组在实验室模拟汽车尾气处理,设计了下图所示装置(部分夹持装置已略去)。
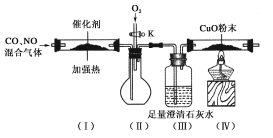
(1)装置(Ⅲ)的主要作用为________________________。
(2)停止加热,打开活塞K,放入适量氧气时,装置(Ⅱ)中可观察到的现象是___________________。
(3)该套装置中有不完善之处,还应在装置(Ⅳ)后补充____________。
(4)工业上常用纯碱液来吸收NOx,有关反应的化学方程式为2NO2+Na2CO3===NaNO2+NaNO3+CO2、NO2+NO+Na2CO3===2NaNO2+CO2。现有标准状况下a L NO2和b L NO的混合气体恰好被200 mL Na2CO3溶液完全吸收,则a、b应满足的关系为________。Na2CO3溶液的物质的量浓度为________mol·L-1(不必化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】区别乙醇、苯和溴苯,最简单的方法是( )
A. 加入金属钠B. 加酸性高锰酸钾溶液后振荡,静置
C. 加蒸馏水后振荡,静置D. 加硝酸银溶液后振荡,静置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是

A. 若A为浓H2SO4,B为Na2SO3,C中盛有Na2SiO3溶液,C中溶液出现白色沉淀,证明非金属性S>Si
B. 若A为浓盐酸,B为MnO2,C中盛有KI淀粉溶液,C中溶液变蓝色
C. 若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,C中先产生白色沉淀后沉淀又溶解
D. 若A为H2O2,B为MnO2,C中盛有Na2S溶液,C中溶液变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯和乙醇的混合气体VL,完全燃烧后生成二氧化碳和水,消耗相同状态下的氧气3VL,则混合气体中乙烯和乙醇的体积比是( )
A. 1∶1B. 2∶1C. 1∶2D. 任意比
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com