
【题目】几种短周期元素的原子半径及主要化合价如下表,下列说法正确的是
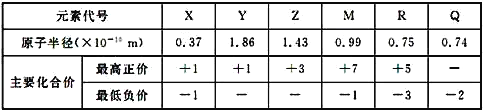
A. 离子半径:Y>Z>M
B. Y、Z、M三种元素的最高价氧化物的水化物两两之间会反应
C. 化合物XM、YM都是电解质.熔融状态下都能导电
D. 气态氢化物稳定性R>Q
【答案】B
【解析】
短周期元素,由元素的化合价可知,Q只有最低价-2价,则Q为O元素;M元素有最高价+7,最低-1,故M为Cl;R有+5、-3价,处于ⅤA族,原子半径小于Cl,且与O元素相近,与氧元素同周期,故R为N元素;Z的最高化合价为+3,没有负化合价,处于ⅢA族,且原子半径Z>Cl,处于第三周期,故Z为Al,X、Y均有最高正价+1,处于IA则,而X有-1价,则X为H元素,Y的原子半径比Al的大很多,可知Y为Na;
A.电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故离子半径Cl->Na+>Al3+,故A错误;
B.Y、Z、R的最高价氧化物的水化物分别为氢氧化钠、氢氧化铝、高氯酸,两两之间可以相互反应,故B正确;
C.化合物XM、YM分别为HCl、NaCl,都是电解质,HCl属于共价化合物,熔融状态下不能导电,故C错误;
D.R为N元素,Q为O元素,气态氢化物稳定性NH3<H2O,故D错误;
答案:B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数之和等于B的质量数,B元素的原子核内质子数等于中子数,下列叙述正确的是( )
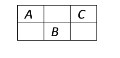
A. B为第二周期的元素
B. C为VA族元素
C. 三种元素都为非金属元素
D. B是三者中化学性质最活泼的非金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物X的合成路线如下图所示。请回答下列问题:
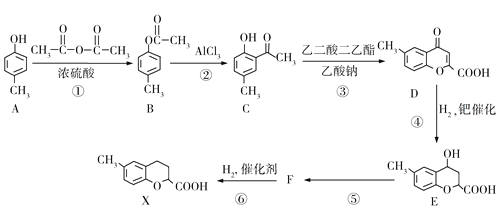
(1)A的名称是________________,X的分子式为_____________。
(2)B的核磁共振氢谱中所有峰的面积之比是________________。
(3)有机物D中含氧官能团的名称是________________,④的反应类型为________________。
(4)反应①的化学方程式为________________________________。
(5)有机物F的结构简式为________________________________。
(6)满足下列条件的C的同分异构体有_____种,任写出其中一种的结构简式_________。
①苯环上只有三个取代基;
②能与三氯化铁溶液反应显色;
③可以发生银镜反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D的原子序数依次增大,B和D同主族;X、Y、N分别是由以上四种元素中两种组成的化合物,Z是由以上三种元素组成的化合物;若X与Y摩尔质量相同,Y为淡黄色固体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定正确的是( )
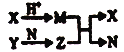
A. 相对分子质量M>N,沸点M>N B. 简单离子半径:D>B>C>A
C. Z 为 Na2CO3 D. 图中有两个氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是重要的核工业原料。下列有关
是重要的核工业原料。下列有关![]() 、
、![]() 说法正确的是
说法正确的是
A. ![]() 原子核中含有92个中子 B.
原子核中含有92个中子 B. ![]() 原子核外有143个电子
原子核外有143个电子
C. ![]() 与
与![]() 互为同位素 D.
互为同位素 D. ![]() 与
与![]() 互为同素异形体
互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式2SO2(g)+O2(g)![]() 2SO3(g) ΔH =QkJ/mol(Q>0),则下列说法正确的是
2SO3(g) ΔH =QkJ/mol(Q>0),则下列说法正确的是
A. 2 molSO2(g)和1 mol O2(g)具有的能量小于2molSO3(g)具有的能量
B. 2molSO2(g)和1molO2(g)置于密闭容器中充分反应放出QkJ的热量
C. 2mol SO2(g)和1molO2(g)置于密闭容器中充分反应放出热量大于QkJ
D. 如将一定量SO2(g)和O2(g)置于密闭容器中充分反应放热量QkJ,则此过程中有2 mol SO2(g)被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2===4CuSO4+2H2O,该反应的还原剂是________________。当1 mol O2发生反应时,还原剂所失电子的物质的量为_________mol。
(2)焙烧明矾的化学方程式为4KAl(SO4)2·12H2O+3S===2K2SO4+2Al2O3+9SO2+48H2O,在该反应中,还原剂是_____________。
(3)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:________________________。
(4)实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
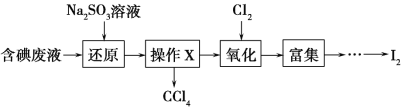
向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为_________________;该操作将I2还原为I-的目的是________________________。
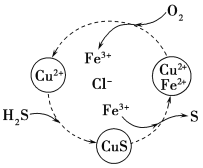
(5)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。在图示的转化中,化合价不变的元素是________________。
(6)NaBH4是一种重要的储氢载体,能与水反应得到NaBO2,且反应前后B的化合价不变,该反应的化学方程式为________________,反应消耗1 mol NaBH4时转移的电子数目为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用如下图所示装置进行有关实验。
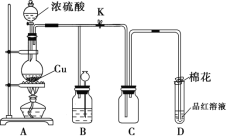
(1)装置A中发生反应的化学方程式为_________________________________________;
(2)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是________________,B中应放置的溶液是________(填字母);
a.水 b.酸性KMnO4溶液 c.浓溴水 d.饱和NaHSO3溶液
(3)若装置C中盛有酸性KMnO4溶液,反应现象为_____________________,体现该气体的_____________(填“氧化性”或“还原性”);
(4)装置D中试管口放置的棉花应浸一种溶液,这种溶液是_____________,其作用是___________;
(5)实验中,取一定质量的铜片和一定体积18 mol·L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,其原因是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com