
| A.离子半径:Clˉ> F ˉ> Na+ > Al3+ |
| B.熔点:石英>食盐>冰>干冰 |
| C.结合氢离子的能力:SO42ˉ> SO32ˉ> CO32ˉ |
| D.热稳定性: HF > HCI > H2S > PH3 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有第2列元素的原子最外层有2个电子 |
| B.第14列元素形成化合物种类最多 |
| C.第3列元素种类最多 |
| D.第17、18列元素都是非金属元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.热稳定性:纯碱>石灰石>小苏打>碳酸 |
| B.除Li外其它碱金属单质均可以保存在煤油中 |
| C.碱金属都是活泼的金属元素,其盐都不发生水解 |
| D.最高氧化物对应水化物碱性LiOH<NaOH<KOH<RbOH<CsOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.最外层有2e-一定在ⅡA |
| B.Na2O2中阴阳离子个数比为1:1 |
| C.CO2各原子最外层都满足8e-的稳定结构 |
| D.ⅦA的氢化物的熔沸点随着相对分子质量的增加而逐渐升高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
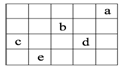
| A.b元素除0价外,只有一种化合价 |
| B.五种元素中,c元素的性质最稳定 |
| C.相同条件下b和d气态氢化物溶于水,溶液的酸性:d<b |
| D.e元素最高价氧化物的水化物和不同量的氧氧化钠溶液反应,可能生成三种盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com