
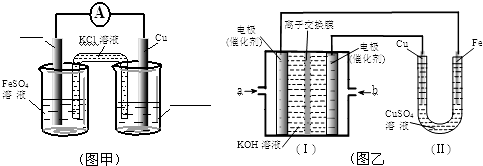
分析 (1)加入稀硫酸是为了抑制Cu2+的水解;
(2)①铁铜原电池中Fe为负极;②铁上镀铜,铜作阳极,铁作阴极;②a为甲烷,b为氧气,据电解质溶液显碱性书写电极反应式;阳极产生的气体为氯气,其体积为448mL(标准状况下),据此计算生成NaOH的物质的量,计算pH;
(3)沉淀转移的方向是向着更难溶的方向移动,通过Ksp的大小可知那种物质更加难溶.
解答 解:(1)CuSO4溶液中铜离子能够水解生成沉淀,加入硫酸是抑制铜离子水解,离子方程式为:Cu2++2H2O?Cu(OH)2+2H+,
故答案为:Cu2++2H2O?Cu(OH)2+2H+;
(2)①图乙在Fe上镀铜,所以Fe作阴极,故答案为:
②图乙在Fe上镀铜,所以Fe作阴极,则连接的为燃料电池的负极,应通入CH4,b极通入O2发生还原反应:O2+4e-+2H2O=4OH-;电解池中均为惰性电极时,阳极的电极反应式为:2Cl--2e-=Cl2↑,阴极反应式为:2H++2e-=H2↑.由电极反应式计算消耗的H+为0.04mol,则生成的OH-为0.04mol,c(OH-)=0.1mol/L,则c(H+)=10-13mol/L,pH=13,故答案为:CH4;O2+4e-+2H2O;13;
(3)由于Ksp(FeS)>Ksp(CuS),所以在相同条件下CuS的溶解度更小,沉淀会向着生成CuS的方向进行,故离子方程式为FeS(s)+Cu2+(aq)=CuS(s)+Fe2+(aq),Cu2+与S2-反应可生成溶度积更小的CuS沉淀,使得上述溶解平衡继续向右移动,
故答案为:存在溶解平衡:FeS(s)?Fe2+(aq)+S2-(aq),其中的Cu2+与S2-生成了溶度积更小的CuS沉淀,使得上述溶解平衡继续向右移动.[或用平衡FeS(s)+Cu2+(aq)=CuS(s)+Fe2+(aq)解释]
点评 本题考查了盐类水解、原电池原理及计算、难溶电解质的沉淀溶解平衡,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 100g•mol-1 | B. | 108g•mol-1 | C. | 55g•mol-1 | D. | 96g•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
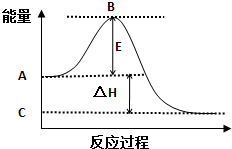 2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.
2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 利用如图所示的装置和其他必要的仪器用品,完成下列实验.
利用如图所示的装置和其他必要的仪器用品,完成下列实验.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
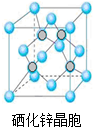 【化学-选修3物质结构与性质】
【化学-选修3物质结构与性质】查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水含镁,将金属钠放入海水中可以制取金属镁 | |
| B. | 从海水中提取溴的过程涉及氧化还原反应 | |
| C. | 利用潮汐能发电是将化学能转化为电能 | |
| D. | 海底多金属结核矿含有Fe、Mn、Co、B等金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同一能层的px、py、pz轨道电子能量相同 | |
| B. | 3d3表示3d能级有3个轨道 | |
| C. | p轨道电子能量不一定高于s轨道电子能量 | |
| D. | 在离核最近区域内运动的电子能量最低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
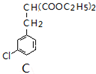 $\underset{\stackrel{①O{H}^{-},②{H}_{3}{O}^{+}}{→}}{③△}$D$\stackrel{SOCl_{2}}{→}$
$\underset{\stackrel{①O{H}^{-},②{H}_{3}{O}^{+}}{→}}{③△}$D$\stackrel{SOCl_{2}}{→}$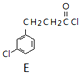 $\stackrel{AlCl_{3}}{→}$
$\stackrel{AlCl_{3}}{→}$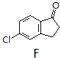
 或
或 (任写一种).
(任写一种). .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题


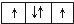


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com