
| 68.2 |
| 12 |
| 13.6 |
| 1 |
| 100-68.2-13.6 |
| 16 |
 ,官能团为醚键,
,官能团为醚键, ;醚键;
;醚键;

 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:
A、硫原子的原子结构示意图: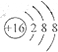 | ||
B、CH4分子的比例模型: | ||
| C、乙烯的结构简式:CH2CH2 | ||
D、原子核内有10个中子的氧原子:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Zn、Fe |
| B、Zn、Ag |
| C、Al、Cu |
| D、Mg、Al |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、14.3g |
| B、25.4g |
| C、28.6g |
| D、50.8g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
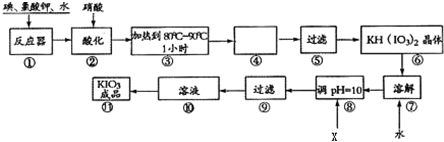
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com