
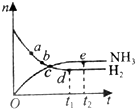
| A�� | ƽ��ʱ�������������䣬�����¶ȿ�ʹ�÷�Ӧ��ƽ�ⳣ������ | |
| B�� | ƽ��ʱ�������������䣬���� NH3 ��Ũ�ȣ������е��������ת���ʼ�С | |
| C�� | �����������䣬ʹ�ø�Ч�����������е��������ת�������� | |
| D�� | ��λʱ�������� NO �� N2 �����ʵ�����Ϊ 1��2 ʱ����Ӧ�ﵽƽ�� |
���� A��ƽ�ⳣ��ֻ���¶�Ӱ�죬��ƽ���ƶ��ķ����ж�ƽ�ⳣ���ı仯��
B�����淴Ӧ�У�����һ�ַ�Ӧ�ƽ�����������ƶ���
C�������ܼӿ췴Ӧ���ʣ�����Ӱ��ƽ����ƶ���
D����Ӧ�ﵽƽ��ʱ����ͬ���ʱ�ʾ�������淴Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�
��� �⣺A������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С����A����
B������һ�ַ�Ӧ��Ũ�ȣ�������Ӧ��ת�������������� NH3 ��Ũ�ȣ������е��������ת��������B����
C��ʹ�ô���ƽ�ⲻ�ƶ��������е��������ת���ʲ��䣬��C����
D����λʱ��������NO��N2�����ʵ�����Ϊ1��2ʱ�����ڻ�ѧ������֮�ȣ���Ӧ����ƽ�⣬��D��ȷ��
��ѡD��
���� ���⿼����������Ի�ѧ��Ӧ�����Լ�ƽ���ƶ���Ӱ��ȣ�����ʱע��ƽ�ⳣ���ı仯�Լ�ƽ��״̬���жϷ�������Ŀ�ѶȲ�����������������ѧ���ķ����������������Ի���֪ʶ��Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �� | C�� | �ڢۢ� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | �������� | ���� |
| ʵ��1 | 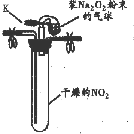 �ٰ���ͼ��װ��������K���������е�Na2O2��ĩ�����Թ��У�����ַ�Ӧ | �Թ��ں���ɫ��ʧ�������� |
| ���Թ���ȴ����������5mL����ˮ | δ������ɫ���壬�Թܵײ�����ȫ���ܽ�ó�����Һ |
| ��� | �������� | ���� |
| ʵ��2 | ȡʵ��1������Һ�� �����м�������MnO2��ĩ�������ٲ������ݺ��ú�ȡ�ϲ���Һ���ٵ��ڴ���ҺpH��7���� | / |
| ʵ��3 | ȡʵ��2�����Һ2mL������2��0.1%������KMnO4��Һ |
| ��� | �������� | ���� |
| ʵ��4 | �����Թ��м���2mL����FeSO4��Һ���ټ���10��0.1mol•L-1NaNO3��Һ���������Թ��м���0.5mL98%��Ũ���� | ����NaNO3��Һ�������Ա仯������Ũ�������Һ����ɫ |
| �����Թ��м���2mL����FeSO4��Һ���ټ���10��0.1mol•L-1NaNO2��Һ���������Թ��м���0.5mL98%��Ũ���� | ����NaNO2��Һ����������ɫ������Ũ�������Һ�����Ա仯 | |
| �����Թ��м���2mL����FeSO4��Һ���ټ���10��ʵ��2�����Һ�����ټ�0.5mL98%��Ũ���� | �μ�ʵ��2�õ�����Һ����Һ������dz��ɫ������Ũ�������Һ������ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ȷ�Ӧ�ڳ����¾����Է����� | |
| B�� | ��֪��ӦCH4��g��+2O2��g��=CO2��g��+2H2O��g����H=-802.3kJ/mol��˵�������ȼ����Ϊ802.3kJ/mol | |
| C�� | ��Ӧ�ȵĴ�С�뷴Ӧ���������ļ����� | |
| D�� | ��1molNaOH����Һ�ֱ�ͺ�0.5molH2SO4��1mol HNO3����Һ��Ӧ���ų���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
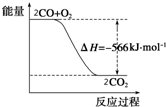 ��֪��2CO��g��+O2��g���T2CO2��g����H=-566kJ•mol-1
��֪��2CO��g��+O2��g���T2CO2��g����H=-566kJ•mol-1| A�� | CO��ȼ����Ϊ566 kJ•mol-1 | |
| B�� | ��ͼ�ɱ�ʾ��CO����CO2�ķ�Ӧ�����������仯�Ĺ��� | |
| C�� | 2Na2O2��s��+2CO2��s���T2Na2CO3��s��+O2��g����H=-452 kJ/mol | |
| D�� | CO��g����Na2O2��s����Ӧ�ų�509 kJ����ʱ������ת����Ϊ2 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3v��A��=2v��C��=0.16 mol/��L•min�� | |
| B�� | �ÿ��淴Ӧ��ƽ��ų�0.8a kJ�����ܣ����軯ѧ��ȫת��Ϊ���ܣ� | |
| C�� | �����¶ȣ���ƽ���������ʼ�С����ƽ�������ƶ� | |
| D�� | ʹ�ô�������С�����������ƽ��������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����� | B�� | ������ | C�� | ��ԭ�� | D�� | ���� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com