
| ||
| �� |
| 11.2L |
| 22.4L/mol |
| 4.48L |
| 22.4L/mol |
| 0.1mol |
| 0.2mol |


 �����ҵ��ٿ���������������ϵ�д�
�����ҵ��ٿ���������������ϵ�д� �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2012�콭��ʡ�����з�����ѧ������һ��ȫ��ģ����Ի�ѧ�Ծ����������� ���ͣ������
��12�֣���������ͳ������dz�������ɫ���������ڹ�ҵ������������Ҫ����;��
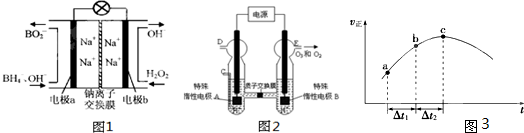
��1���ݱ��������⻯����NaBH4��B�Ļ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ�������ͨ�����ǵ�Դ���������ϲ���Pt/C���������ϲ���MnO2���乤��ԭ����ͼ7��ʾ���õ�طŵ�ʱ�����ĵ缫��ӦʽΪ�� ����MnO2���������ϣ���������Ϊ ��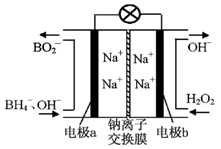
��2��������䳣��Һ̬�£�N2H4��Ϊȼ�ϣ�Һ̬��������Ϊ��ȼ����
��֪��N2H4(g) + O2(g) �� N2(g) + 2H2O(g) ��H =" �C" 534 kJ��mol��1
H2O2(l) = H2O(l) + 1/2O2(g) ��H =" �C" 98.64 kJ��mol��1
H2O(l) = H2O(g) ��H=" +" 44kJ��mol��1
��ӦN2H4(g) + 2H2O2(l) = N2(g) + 4H2O(g) �ġ�H= ��
��3��O3 ���ɳ�����������ԭ����ͼ��ʾ�����ϡ�����Ƶá�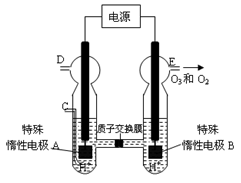
��ͼ������Ϊ ���A����B������
����C��ͨ��O 2����A���ĵ缫��ӦʽΪ�� ��
����C����ͨ��O 2 ��D��E���ֱ��ռ���11.2L����4.48L���壨��״���£�����E���ռ���������O3��ռ���������Ϊ ������ O 3 �ķֽ⣩�� ��4������O3����������ȼú�����е�NOx��SO2�ѳ�Ч����������¯�����е�NOx 95����������NO��ʽ���ڵģ��ɷ�����ӦNO(g��+ O3 (g) NO2(g)+ O2 (g)����һ�������£���NO��O3ͨ����Ⱥ����ܱ������з���������Ӧ������Ӧ������ʱ��仯��ʾ��ͼ����ͼ9����ʾ����ͼ�ɵó�����ȷ˵����
��4������O3����������ȼú�����е�NOx��SO2�ѳ�Ч����������¯�����е�NOx 95����������NO��ʽ���ڵģ��ɷ�����ӦNO(g��+ O3 (g) NO2(g)+ O2 (g)����һ�������£���NO��O3ͨ����Ⱥ����ܱ������з���������Ӧ������Ӧ������ʱ��仯��ʾ��ͼ����ͼ9����ʾ����ͼ�ɵó�����ȷ˵���� 
a����Ӧ��c��ﵽƽ��״̬
b����Ӧ��Ũ�ȣ�b��С��c��
c����Ӧ��������������������������
d����t1����t2ʱ��NO��ת���ʣ�a��b��С��b��c��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�콭��ʡ�γ���������ѧ������ѧ��ѧ����п��Ի�ѧ�Ծ����������� ���ͣ������
(14 ��)��������ͳ������dz�������ɫ���������ڹ�ҵ������������Ҫ����;��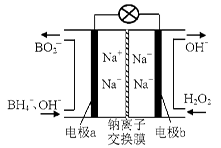
��1���ݱ��������⻯����NaBH4��B�Ļ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ�������ͨ�����ǵ�Դ���������ϲ���Pt/C���������ϲ���MnO2���乤��ԭ������ͼ��ʾ���õ�طŵ�ʱ�����ĵ缫��ӦʽΪ�� ��
��MnO2���������ϣ���������Ϊ ��
��2��������䳣��Һ̬�£�N2H4��Ϊȼ�ϣ�Һ̬��������
Ϊ��ȼ������֪��
N2H4(g) + O2(g) �� N2(g) + 2H2O(g) ��H =" �C" 534 kJ��mol-1
H2O2(l) = H2O(l) + 1/2O2(g) ��H =" �C" 98.64 kJ��mol-1
H2O(l) = H2O(g) ��H=" +" 44kJ��mol-1
��ӦN2H4(g) + 2H2O2(l) = N2(g) + 4H2O(g) �ġ�H= ��
��3��O3 ���ɳ�����������ԭ������ͼ��ʾ�����ϡ�����Ƶá�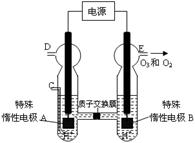
�� ͼ������Ϊ ���A����B������
����C��ͨ��O 2����A���ĵ缫��ӦʽΪ�� ��
����C����ͨ��O 2 ��D��E���ֱ��ռ���15.68L����6.72L���壨��״���£�����E���ռ���������O2��O3�����֮��Ϊ ������ O 3 �ķֽ⣩��
��4������O3����������ȼú�����е�NOx��SO2�ѳ�Ч����������¯�����е�NOx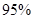 ��������NO��ʽ���ڵģ��ɷ�����ӦNO(g��+ O3 (g)
��������NO��ʽ���ڵģ��ɷ�����ӦNO(g��+ O3 (g) 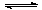 NO2(g)+ O2 (g)����һ�������£���NO��O3ͨ����Ⱥ����ܱ������з���������Ӧ ������Ӧ������ʱ��仯��ʾ��ͼ������ͼ����ʾ����ͼ�ɵó�����ȷ˵����
NO2(g)+ O2 (g)����һ�������£���NO��O3ͨ����Ⱥ����ܱ������з���������Ӧ ������Ӧ������ʱ��仯��ʾ��ͼ������ͼ����ʾ����ͼ�ɵó�����ȷ˵���� 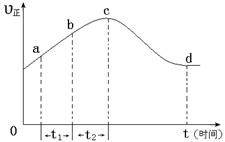
a����Ӧ��c��ﵽƽ��״̬
b����Ӧ��Ũ�ȣ�b��С��c��
c���÷�ӦΪ���ȷ�Ӧ
d����t1����t2ʱ��NO��ת������a��b��С��b��c��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�꽭��ʡ�γ��и�����ѧ��ѧ����п��Ի�ѧ�Ծ��������棩 ���ͣ������
(14 ��)��������ͳ������dz�������ɫ���������ڹ�ҵ������������Ҫ����;��
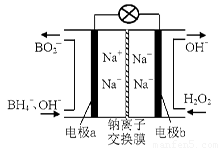
��1���ݱ��������⻯����NaBH4��B�Ļ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ�������ͨ�����ǵ�Դ���������ϲ���Pt/C���������ϲ���MnO2���乤��ԭ������ͼ��ʾ���õ�طŵ�ʱ�����ĵ缫��ӦʽΪ�� ��
��MnO2���������ϣ���������Ϊ ��
��2��������䳣��Һ̬�£�N2H4��Ϊȼ�ϣ�Һ̬��������
Ϊ��ȼ������֪��
N2H4(g) + O2(g) �� N2(g) + 2H2O(g) ��H =" �C" 534 kJ��mol-1
H2O2(l) = H2O(l) + 1/2O2(g) ��H =" �C" 98.64 kJ��mol-1
H2O(l) = H2O(g) ��H=" +" 44kJ��mol-1
��ӦN2H4(g) + 2H2O2(l) = N2(g) + 4H2O(g) �ġ�H= ��
��3��O3 ���ɳ�����������ԭ������ͼ��ʾ�����ϡ�����Ƶá�
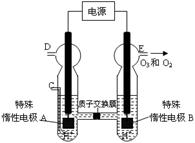
�� ͼ������Ϊ ���A����B������
����C��ͨ��O 2����A���ĵ缫��ӦʽΪ�� ��
����C����ͨ��O 2 ��D��E���ֱ��ռ���15.68L����6.72L���壨��״���£�����E���ռ���������O2��O3�����֮��Ϊ ������ O 3 �ķֽ⣩��
��4������O3����������ȼú�����е�NOx��SO2�ѳ�Ч����������¯�����е�NOx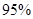 ��������NO��ʽ���ڵģ��ɷ�����ӦNO(g��+ O3 (g)
��������NO��ʽ���ڵģ��ɷ�����ӦNO(g��+ O3 (g)  NO2(g)+ O2 (g)����һ�������£���NO��O3ͨ����Ⱥ����ܱ������з���������Ӧ ������Ӧ������ʱ��仯��ʾ��ͼ������ͼ����ʾ����ͼ�ɵó�����ȷ˵����
NO2(g)+ O2 (g)����һ�������£���NO��O3ͨ����Ⱥ����ܱ������з���������Ӧ ������Ӧ������ʱ��仯��ʾ��ͼ������ͼ����ʾ����ͼ�ɵó�����ȷ˵����
a����Ӧ��c��ﵽƽ��״̬
b����Ӧ��Ũ�ȣ�b��С��c��
c���÷�ӦΪ���ȷ�Ӧ
d����t1����t2ʱ��NO��ת������a��b��С��b��c��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�꽭��ʡ�����и�����һ��ȫ��ģ����Ի�ѧ�Ծ��������棩 ���ͣ������
��12�֣���������ͳ������dz�������ɫ���������ڹ�ҵ������������Ҫ����;��
��1���ݱ��������⻯����NaBH4��B�Ļ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ�������ͨ�����ǵ�Դ���������ϲ���Pt/C���������ϲ���MnO2���乤��ԭ����ͼ7��ʾ���õ�طŵ�ʱ�����ĵ缫��ӦʽΪ�� ����MnO2���������ϣ���������Ϊ ��
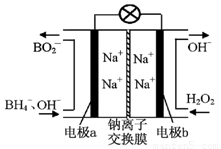
��2��������䳣��Һ̬�£�N2H4��Ϊȼ�ϣ�Һ̬��������Ϊ��ȼ����
��֪�� N2H4(g) + O2(g) �� N2(g) + 2H2O(g) ��H = �C 534 kJ��mol��1
H2O2(l) = H2O(l) + 1/2O2(g) ��H = �C 98.64 kJ��mol��1
H2O(l) = H2O(g) ��H= + 44kJ��mol��1
��ӦN2H4(g) + 2H2O2(l) = N2(g) + 4H2O(g) �� ��H= ��
��3��O3 ���ɳ�����������ԭ����ͼ��ʾ�����ϡ�����Ƶá�
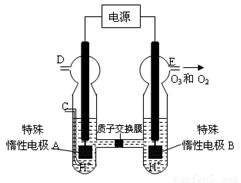
��ͼ������Ϊ ���A����B������
����C��ͨ��O 2����A���ĵ缫��ӦʽΪ�� ��
����C����ͨ��O 2 ��D��E���ֱ��ռ���11.2L����4.48L���壨��״���£�����E���ռ���������O3��ռ���������Ϊ ������ O 3 �ķֽ⣩��
 ��4������O3����������ȼú�����е�NOx��SO2�ѳ�Ч����������¯�����е�NOx 95����������NO��ʽ���ڵģ��ɷ�����ӦNO(g��+ O3
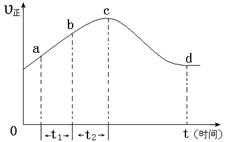
(g) NO2(g)+ O2 (g)����һ�������£���NO��O3ͨ����Ⱥ����ܱ������з���������Ӧ ������Ӧ������ʱ��仯��ʾ��ͼ����ͼ9����ʾ����ͼ�ɵó�����ȷ˵����
��4������O3����������ȼú�����е�NOx��SO2�ѳ�Ч����������¯�����е�NOx 95����������NO��ʽ���ڵģ��ɷ�����ӦNO(g��+ O3
(g) NO2(g)+ O2 (g)����һ�������£���NO��O3ͨ����Ⱥ����ܱ������з���������Ӧ ������Ӧ������ʱ��仯��ʾ��ͼ����ͼ9����ʾ����ͼ�ɵó�����ȷ˵����
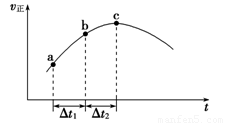
a����Ӧ��c��ﵽƽ��״̬
b����Ӧ��Ũ�ȣ�b��С��c��
c����Ӧ��������������������������
d����t1����t2ʱ��NO��ת���ʣ�a��b��С��b��c��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com