
 FeO (s) + CO (g)的平衡常数为K1,
FeO (s) + CO (g)的平衡常数为K1, FeO (s) + H2 (g)的平衡常数为K2,
FeO (s) + H2 (g)的平衡常数为K2,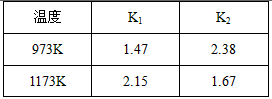
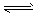 CO (g) + H2O (g),写出该反应的平衡常数K3的数学表达式______________。
CO (g) + H2O (g),写出该反应的平衡常数K3的数学表达式______________。 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
 2NH3是工业上合成氨的重要反应.
2NH3是工业上合成氨的重要反应.
 2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/mol
2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/mol 2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/mol
2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/mol| 16 |
| a2 |
| 16 |
| a2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
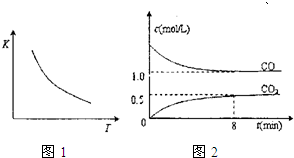 (2010?沈阳二模)一定条件下某密闭容器中发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g),已知该反应的平衡常数(K)的与温度(T)的关系如图1,图2是T1温度下该反应的c-t关系图象.则下列说法正确的是( )
(2010?沈阳二模)一定条件下某密闭容器中发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g),已知该反应的平衡常数(K)的与温度(T)的关系如图1,图2是T1温度下该反应的c-t关系图象.则下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| ||
| 实验步骤 | 实验现象 | 用化学用语解释 |
| 将少量气体通入淀粉KI溶液 | 溶液最初变成 蓝 蓝 色 |
Cl2+2I-=I2+2Cl- Cl2+2I-=I2+2Cl- (用离子方程式表示) |
| 继续通入气体 | 溶液逐渐变成无色 | 5Cl2+I2+6H2O=2HIO3+10HCl 5Cl2+I2+6H2O=2HIO3+10HCl (用化学方程式表示) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com