
ijѧ���к͵ζ�ʵ�����Ϊ��(a)ȡ��ʽ�ζ��ܣ�(b)������ˮϴ����(c)������������NaOH��Һ��(d)��¼Һ��̶ȶ�����(e)����ʽ�ζ��ܾ�ȷ�ų�һ��������Һ���뵽ֻ������ˮϴ�ӹ�����ƿ�У�(f)����ƿ�м�����������ˮ��(g)�����̪��Һ2�Σ�(h)�ζ�ʱ��ҡ����ƿ��(i)��ע�ӵζ�����Һ��仯��(j)���ε���Һ����ɫ�䵽�ۺ�ɫʱ������ֹͣ�ζ���(k)��¼Һ��̶ȶ�����(m)�����ظ����εζ��ĺ�NaOH��Һ���ƽ��ֵΪ22mL������ʵ������д���֮����(����)
A��c��d��f��j��k B��c��i��j��m
C��e��f��i��m D��c��e��f��i��j��m
 �ܿ�����ĩ��̾�ϵ�д�
�ܿ�����ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������ʵ���ҳ���������ɳ����ԭ�����͵���
A������ˮ�д�������ƽ�⣺ ��������NaOH��Һ����ɫ��dz
��������NaOH��Һ����ɫ��dz
B����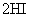

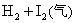 ƽ����ϵ����ѹǿʹ��ɫ����
ƽ����ϵ����ѹǿʹ��ɫ����
C����Ӧ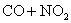

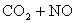 �����¶�ʹƽ�����淽���ƶ�
�����¶�ʹƽ�����淽���ƶ�
D���ϳɰ���Ӧ��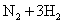

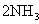 ��Ϊʹ���IJ�����ߣ�������Ӧ��ȡ���¸�ѹ�Ĵ�ʩ
��Ϊʹ���IJ�����ߣ�������Ӧ��ȡ���¸�ѹ�Ĵ�ʩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ࡢ֬���͵�������ά����������������������Ӫ�����ʡ�����������ȷ���� �� ��
A.ֲ���Ͳ��ܷ���ˮ�ⷴӦ B.����ˮ������ղ�����������
C.�������ܷ���������Ӧ��ˮ�ⷴӦ D.������ˮ��IJ���Ϊ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ�ķ�Ӧ�Ȧ�H>0����
A���������������ᷴӦ B�����������������Ȼ�淋ķ�Ӧ
C��п������ķ�Ӧ D��̼��ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ����( )
��CH3OH(g)��H2O(g)��CO2(g)��3H2(g) ��H ����49.0 kJ/mol
��CH3OH(g)��1/2O2(g)��CO2(g)��2H2(g) ��H����192.9 kJ/mol
����������Ӧ������˵����ȷ����
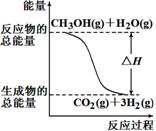
A. ��Ӧ���е������仯����ͼ��ʾ
B. ����֪2H2(g)��O2(g)��2H2O(g)
��H����483.8 kJ/mol
C. 1 mol CH3OH���ȼ�շų�������Ϊ192.9 kJ
D. CH3OHת���H2�Ĺ���һ��Ҫ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���淴Ӧ��2NO2(g) 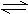 2NO(g)��O2(g)������̶����ܱ������н��У����жϴﵽƽ��״̬�ı�־���ǣ� ��
2NO(g)��O2(g)������̶����ܱ������н��У����жϴﵽƽ��״̬�ı�־���ǣ� ��
�ٵ�λʱ��������n mol O2��ͬʱ����2n mol NO2��
������O2�����ʵ�������NO2�����ʡ�
����NO2��NO��O2��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬
�ܻ���������ɫ���ٸı��״̬��
�ݻ��������ܶȲ��ٸı��״̬��
��������ѹǿ���ٸı��״̬��
��������ƽ����Է����������ٸı��״̬
A���٢ܢޢ� B ���ڢۢ� C���٢ۢܢ� D��ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���г���ʱpH=1��ijǿ����Һ10 mL�����в�����ʹ��ҺpH���2����
A����ˮϡ�ͳ�100 mL B������10 mLˮ����ϡ��
C������10 mL 0.01 mol��L-1��NaOH��Һ D������10 mL 0.01 mol��L-1��HCI��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������������ʼ��仯�����ڹ�ҵ���й㷺Ӧ�á�
��1��ͬ��ʯ�ڸ������Ʊ������Ȼ�ѧ����ʽΪ��
 4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g) H
H
��֪��ͬ�����£�
4Ca3(PO4)2F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g) ��H1
2Ca3(PO4)2(s)+10C(s)=P4(g)+6CaO(s)+10CO(g) ��H2
SiO2(s)+CaO(s)=CaSiO3(s) ��H3
�á�H1����H2�͡�H3��ʾ H����
H���� H=____________________��
H=____________________��
��2�������������Ϊ����������ӣ�����ṹʽ��ͼ��֮����ȥ����ˮ���Ӳ����ṹʽΪ________________________________�����������ƣ��׳ơ����ơ����dz��õ�ˮ���������仯ѧʽΪ____________��
��3���������ƣ�NaH2PO2�������ڹ�ҵ�ϵĻ�ѧ������
�ٻ�ѧ��������Һ�к���Ni2+��H2PO2���������Ե������·���������Ӧ��
��a��_____ Ni2+ + ____ H2PO2��+ _____ �� ___Ni++______ H2PO3��+ ____
��b��6H2PO-2 +2H+ =2P+4H2PO3+3H2��
���ڴ����д������ƽ��Ӧʽ��a����
�����â��з�Ӧ�������϶Ƽ�������������Ͻ𣬴Ӷ��ﵽ��ѧ������Ŀ�ģ�����һ�ֳ����Ļ�ѧ�ơ�������·���Ƚϻ�ѧ�����ơ�
�����ϵIJ�ͬ�㣺______________________________________________________��
ԭ���ϵIJ�ͬ�㣺______________________________________________________��
��ѧ�Ƶ��ŵ㣺________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з����п���֤��2HI������ H2������+I2�������Ѵ�ƽ��״̬����
H2������+I2�������Ѵ�ƽ��״̬����
�� ��λʱ��������n mol H2��ͬʱ����n mol HI
�� һ��H-H�����ѵ�ͬʱ������H-I������
���¶Ⱥ�ѹǿһ��ʱ��������ܶȲ��ٱ仯
�� ��Ӧ���ʦԣ�H2��=�ԣ�I2��=0.5�ԣ�HI��ʱ
�� c(HI)=c(H2)=c(I2)=2:1:1
�� �¶Ⱥ����һ��ʱ��ijһ������Ũ�Ȳ��ٱ仯
�� �¶Ⱥ����һ��ʱ��������ѹǿ���ٱ仯
�� ����һ������������ƽ����Է����������ٱ仯
�� �¶Ⱥ����һ��ʱ����������ɫ���ٱ仯
A. �ڢۢܢݢ� B. �ڢޢߢ�� C. �٢ڢޢ� D. �ڢޢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com