
科目:高中化学 来源: 题型:解答题
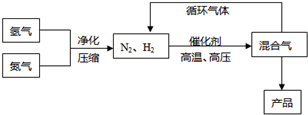
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210.01 | -252.77 | -77.74 |
| 沸点(℃) | -195.79 | -259.23 | -33.42 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
2H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1
现有1g液态H2O,蒸发时吸收的热量是
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
盐酸滴入Na2CO3溶液中,有下列反应: ①Na2CO3+HCl====NaHCO3+NaCl
②NaHCO3+HCl====NaCl+H2O+CO2↑
并将含有HCl 0.2 mol的稀盐酸,加入含Na2CO3 0.14 mol的溶液中,经充分反应后,溶液中各物质的量是Na2CO3______HCl______NaCl______NaHCO3______
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com