
煤是我国城乡居民普遍使用的一种家用能源.烟煤中含有硫化物(FeS2),燃烧可产生SO2,设某40万人口的中等城市,每人每天燃煤5 kg,假设某煤中FeS2的质量分数为5%,燃烧时有90%的硫转化为SO2,被排放到大气中.FeS2燃烧的反应式为4FeS2+11O2![]() 2Fe2O3+8SO2.问:
2Fe2O3+8SO2.问:
(1)燃烧1吨煤可产生多少千克SO2?
(2)该城市若全部以这种烟煤作燃料,每年(按365天计算)将有多少吨SO2排放到大气中?
(3)下雨时测定其雨水呈酸性,写出反应式:__________________.
(4)测定某份雨水样品,每隔一定时间测定一次pH,发现pH逐渐变小,其原因是________________.
(5)简述这种雨水将给环境中的生物和非生物造成哪些影响?
(6)你能提出几项减轻这种危害的对策吗?
|
答案:(1)48 kg (2)35 040 t (3)SO2+H2O (4)H2SO3被空气中的O2氧化为强酸H2SO4 (5)酸雨可腐蚀金属、建筑物,破坏植物,污染湖泊,导致大量鱼类及其他水生生物死亡(未形成酸雨的SO2,可刺激人体的呼吸系统,诱发慢性支气管炎、肺气肿和支气管哮喘等疾病,括号中的可不答). (6)减轻这种自然危害的对策有: ①用烧碱溶液吸收SO2,反应式为:SO2+2NaOH ②种植柳杉、垂柳、臭椿等可吸收SO2的植物; ③减少煤的燃烧,使用清洁燃料. 解析:第(1)小问:抓住反应前后硫元素质量守恒即可,由方程式可知燃烧1 t煤可产生的SO2的质量为: 第(2)小问:每年排放的SO2为:400 000×5 kg×10-3 t·kg-1×365×0.048 t=35 040 t 第(4)小问:空气中有较多O2,H2SO3放置一段时间后,被O2氧化为强酸H2SO4,所以酸性增强. 第(6)小问:联系所学知识,提出解决实际问题的对策,答案不一定唯一,答案中的几种可供参考. |


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源:走向清华北大同步导读·高一化学 题型:043
煤目前是我国城乡居民普遍使用的一种家用能源.烟煤中含有硫化物(FeS2),其燃烧可产生SO2.设某40万人口的中等城市,每户每天烧煤5kg,假设某煤中含FeS2的质量分数为5%,燃烧时有90%的硫转化为SO2被排入大气,其反应式:
4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
(1)燃烧1t可产生多少千克 SO2?
(2)该城市若全部以这种烟煤作燃料,每年(按365天),将有多少t SO2排放到大气?
(3)下雨时测定其雨水呈酸性,写出反应式.
(4)测定某份雨水样品,每隔一定时间测定一次pH,发现pH逐渐变小,其原因是________.

(5)简述这种雨水将给环境中的生物和非生物造成哪些影响?
(6)你能提出两、三项减轻这种危害的对策吗?
查看答案和解析>>
科目:高中化学 来源:龙之脉新教材完全解读 高中化学 必修1 配鲁科版 鲁科版 题型:022
煤是我国城乡居民普遍使用的一种家用能源.烟煤中含FeS2,其燃烧可产生SO2.设某城市有40万户人口,每户每天燃煤5 kg,假设烟煤中FeS2的质量分数为5%,燃烧时有90%的硫转化为SO2排放到大气中.FeS2燃烧时的反应式为:4FeS2+11O2![]() 2Fe2O3+8SO2,问:
2Fe2O3+8SO2,问:
(1)燃烧1t煤可产生多少kg SO2?
(2)该城市若全部以这种烟煤为燃料,每年(按365天)将有多少t SO2排到大气中?
(3)下雨时测定其雨水为酸性,写出其反应式:________.
(4)测定某份雨水样品,每隔一定时间测定一次pH,发现pH逐渐变小,解释其原因:
查看答案和解析>>
科目:高中化学 来源: 题型:038
煤是我国城乡居民普遍使用的一种家用能源.烟煤中含有硫化物(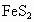 ),其燃烧可产生
),其燃烧可产生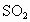 .设某40万户的城市,每户每天燃烧5kg,假设某烟煤中
.设某40万户的城市,每户每天燃烧5kg,假设某烟煤中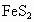 的质量分数为5%,燃烧时有90%的硫转化为
的质量分数为5%,燃烧时有90%的硫转化为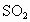 ,被排放到大气中,
,被排放到大气中,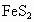 燃烧时的反应式为
燃烧时的反应式为 ,问:
,问:
(1)燃烧1t煤可产生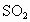 多少千克?
多少千克?
(2)该城市若全部以这种烟煤作燃料,每年(按365天计算),将有多少吨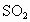 排放到大气中.
排放到大气中.
(3)下雨时测定其雨水呈酸性,写出反应方程式____________________.
(4)测定某份雨水样品,每隔一定时间测定一次pH,发现pH逐渐变小见下表,其原因是:
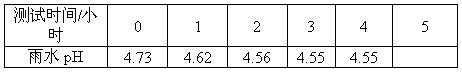
(5)简述这种雨水将给环境中的生物和非生物造成哪些影响?
(6)你能提出两三项减轻这种危害的对策吗?
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)燃烧1吨煤可产生多少千克SO2?
(2)该城市若全部以这种烟煤作燃料,每天(按365天计算),将有多少吨SO2排放到大气中?
(3)下雨时测定其雨水呈酸性,写出反应式:
___________________________________________________________________。
(4)测定某份雨水样品,每隔一定时间测定一次pH,发现pH逐渐变小,其原因是__________
_____________________________________________________________________。
测试时间小时 | 1 | 2 | 3 | 4 | 5 |
雨水pH | 4.73 | 4.62 | 4.56 | 4.5 | 4.55 |
(5)简述这种雨水将给环境中的生物和非生物造成哪些影响?
(6)你能提出两三项减轻这种危害的对策吗?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com