
①2Na2SO3+O2===2Na2SO4(时间不长)
②2H2SO3+O2===2H2SO4(时间较长)
③2SO2+O2![]() 2SO3
2SO3
说明还原性由弱到强的顺序是
A.Na2SO3、H2SO3、SO3、SO2
B.SO2、H2SO3、Na2SO3
C.H2SO3、SO2、Na2SO3
D.Na2SO3、SO2、H2SO3
科目:高中化学 来源: 题型:

| ||
| (2)H+ |


 CH2CH2
CH2CH2 )反应合成PBSA的化学方程式:
)反应合成PBSA的化学方程式:| 一定条件 |
 OC-COO(CH2)4O
OC-COO(CH2)4O H+(2n-1)H2O
H+(2n-1)H2O| 一定条件 |
 OC-COO(CH2)4O
OC-COO(CH2)4O H+(2n-1)H2O
H+(2n-1)H2O

查看答案和解析>>
科目:高中化学 来源: 题型:



| 浓硫酸 |
| 170℃ |
| 浓硫酸 |
| 170℃ |
 +nHOCH2CH2OH
+nHOCH2CH2OH| 浓硫酸 |
| △ |
 +(2n-1)H2O
+(2n-1)H2O +nHOCH2CH2OH
+nHOCH2CH2OH| 浓硫酸 |
| △ |
 +(2n-1)H2O
+(2n-1)H2O查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 部分结构知识 | 部分性质 |
| X | X原子核外电子占有9个原子轨道 | X的一种氧化物是形成酸雨的主要物质 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |


查看答案和解析>>
科目:高中化学 来源: 题型:
①乙+丙![]() 己 ②甲+丙
己 ②甲+丙![]() 庚 ③戊+己
庚 ③戊+己![]() 丁
丁
④戊+庚![]() 丙+辛 ⑤己+庚
丙+辛 ⑤己+庚![]() 丙+辛
丙+辛
若丁的用途如下图所示,试完成下列问题:
(1)写出下列物质的化学式:
己:_______________________________________________________________;
庚:_______________________________________________________________;
丁:_______________________________________________________________。

(2)写出下列反应的化学方程式:
反应③:_____________________________________________________;
反应④:______________________________________________________。
(3)298 K时向体积为V L的真空容器内通入n mol 己和m mol庚。
①若n=2,则当m=_____________时,反应后容器内气体的密度最小。
②若2n>m,则反应后氧化产物与还原产物的质量差为____________________g。
③若5n=m,则反应后氧化产物与还原产物的质量和为48 g,则n+m=_______________。
查看答案和解析>>
科目:高中化学 来源:新疆自治区月考题 题型:单选题
 2N(g)+W(g) ΔH>0,达到平衡时,vA= 1.2a L,则下列说法错误的是
2N(g)+W(g) ΔH>0,达到平衡时,vA= 1.2a L,则下列说法错误的是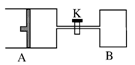
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com