
| A�� | ����ϩ����ʽΪC30H50 | |
| B�� | ����ϩ�����ʽΪC29H48�����ʿ�������ͬϵ�� | |
| C�� | ����ϩ��ȫ�����ΪC30H62 | |
| D�� | 1mol����ϩ������5mol�嵥�ʼӳ� |
���� ����ϩ��������״�ṹ�������к���30��̼ԭ����̼��������Ϊ7.2��1����Hԭ�Ӹ���Ϊx����$\frac{30��12}{x}$=$\frac{7.2}{1}$����ã�x=50������ʽΪC30H50�����л���Ϊ��״�ṹ��ϩ���������Ͷ�Ϊ��$\frac{30��2+2-50}{2}$=6�����Է����к�6��C=C�������ϩ�������ʡ�ͬϵ�������ͨʽ��֪ʶ���н��
��� �⣺����ϩ��������״�ṹ�������к���30��̼ԭ����̼��������Ϊ7.2��1����Hԭ�Ӹ���Ϊx����$\frac{30��12}{x}$=$\frac{7.2}{1}$����ã�x=50������ʽΪC30H50��
A���������ϼ����֪������ϩ����ʽΪC30H50����A��ȷ��
B������ϩ��������״�ṹ�������к���6��̼̼˫��������ʽΪC29H48�����ʣ������Ͷ�ҲΪ6�����ܺ���6��̼̼˫�������߽ṹ�������ƣ��п��ܻ�Ϊͬϵ���B��ȷ��
C��ʵ���ý���ϩ��������״�ṹ����ȫ�����Ӧ���������������ϩ��ȫ���������к���Hԭ����Ϊ��30��2+2=62�����������ʽΪC30H62����C��ȷ��
D������ʽΪC30H50��ʵ���ý���ϩ��������״�ṹ�������Ͷ�Ϊ$\frac{30��2+2-50}{2}$=6��������к�6��C=C����1mol����ϩ������6mol�嵥�ʼӳɣ���D����
��ѡD��
���� ���⿼���л������ʽ��ȷ�����жϣ���Ŀ�Ѷ��еȣ�ע������л���Ĺ����������ʵĹ�ϵ����ȷ��Ϣ����״�ṹ�Ƴ�����ϩ�����к���6��̼̼˫���ǽ��Ĺؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬһ�ֺ��� | B�� | ��Ϊͬ���칹�� | C�� | ��Ϊͬ�������� | D�� | ��Ϊͬλ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��2 | B�� | 1��3 | C�� | 3��2 | D�� | 1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ������� | ��ʼ�����ʵ����ʵ�����mol�� | �ﵽƽ��ʱ�����仯 | ||
| N2 | H2 | NH3 | ||
| �� | 1 | 3 | 0 | �ų�23.15kJ���� |
| �� | 0.9 | 2.7 | 0.2 | �ų�QkJ���� |
| A�� | �����١����з�Ӧ�Ļ�ѧƽ�ⳣ����� | |
| B�� | ƽ��ʱ���������а������������ԼΪ14.3% | |
| C�� | ��Ӧ�ڴﵽƽ��ʱ���ų�������Q=23.15 kJ | |
| D�� | ���ٵ����Ϊ5.0 L����ﵽƽ��ʱ�ų�������С��23.15 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D | |
| ǿ����� | HBr | FeCl3 | H2SO4 | Ca��OH��2 |
| ������� | HF | HCOOH | BaSO4 | HI |
| �ǵ���� | NH3 | Cu | H2O | C2H5OH |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
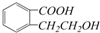 ��������ͨ����ͬ�ķ�Ӧ�õ��������ʣ�
��������ͨ����ͬ�ķ�Ӧ�õ��������ʣ� C��
C�� D��
D�� E��
E��
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 20% | B�� | 40% | C�� | 60% | D�� | 80% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȩ | B�� | �Ҵ� | C�� | �Ҷ��� | D�� | ���� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com