��ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��109g5.51%��NaOH��Һ��������CuSO
4��Һ��200g10.00%��K
2SO
4��Һ���缫��Ϊʯī�缫����ͨ��Դ������һ��ʱ���ñ���K
2SO
4Ũ��Ϊ10.47%������c�缫�������ӣ��ݴ˻ش����⣺
��1���缫b�Ϸ����ĵ缫��ӦΪ______��
��2���缫b�����ɵ������ڱ�״���µ����Ϊ______����ʱ���ձ���NaOH��Һ�����ʵ���Ũ��Ϊ������Һ���ܶ�Ϊ1g/cm
3��______��
��3���缫c�������仯��______g����ʹ�������еĵ��Һ�ָ�����ʼ״̬��Ӧ������Һ�м���������______������ĸ��ţ���
A��Cu��OH��
2 B��Cu
2O C��CuCO
3 D��Cu
2��OH��
2CO
3��4�������������䣬�������װ�ø�Ϊ��⾫��ͭ����c�缫�IJ���Ϊ______��d�缫�IJ���Ϊ______��

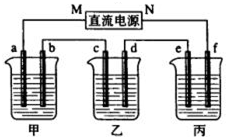


 ��У����ϵ�д�
��У����ϵ�д�

 ��ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��100g 5.00%��NaOH��Һ��������CuSO4��Һ��100g 10.00%��K2SO4��Һ���缫��Ϊʯī�缫��
��ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��100g 5.00%��NaOH��Һ��������CuSO4��Һ��100g 10.00%��K2SO4��Һ���缫��Ϊʯī�缫��

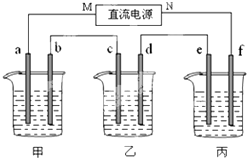 ��ͼ��ʾװ���У��ס��������ձ��ֱ�����ʢ��200mL����ʳ��ˮ��������AgNO3��Һ��a��b��c��d�ĸ��缫��Ϊʯī�缫����ͨ��Դ������һ��ʱ��������d�缫����������2.16g���ݴ˻ش����⣺
��ͼ��ʾװ���У��ס��������ձ��ֱ�����ʢ��200mL����ʳ��ˮ��������AgNO3��Һ��a��b��c��d�ĸ��缫��Ϊʯī�缫����ͨ��Դ������һ��ʱ��������d�缫����������2.16g���ݴ˻ش����⣺