
| A. | 用溴水代替碘水进行萃取实验 | |
| B. | 用过量的氯气进行性质实验 | |
| C. | 用乙烯和氧气在银作催化剂的条件下制备环氧乙烷 | |
| D. | 用铜粉代替铜丝进行铜和浓硝酸反应的实验 |
分析 绿色化学又称“环境无害化学”、“环境友好化学”、“清洁化学”,绿色化学的最大特点是从源头就采用预防污染的科学手段,因而过程和终端均为零排放或零污染,双氧水生成氧气同时生成无污染的水,转化成了期望中的产品,实现了绿色化学的理念,据此解答.
解答 解:A.溴水易挥发、溴蒸气有毒,故不符合绿色化学理念,故A错误;
B.Cl2是有毒气体,用过量的氯气进行性质实验容易引起环境污染,不符合绿色化学理念,故B错误;
C.乙烯在银作催化剂条件下被氧气氧化生成环氧乙烷,原子利用率100%,符合绿色化学理念,故C正确;
D.铜丝进行Cu和浓硝酸的反应,可以控制反应速率,从浓硝酸中移出铜丝反应就会停止,用铜粉无法控制反应速率,不符合绿色化学的理念,故D错误;
故选:C.
点评 本考点考查了绿色化学,理解绿色化学的概念、熟悉相关物质的性质是解答的关键,题目难度不大.


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:选择题
| A. | 2.24LNH3和CH4的混合气体,所含电子总数为2NA | |
| B. | 1mol乙醇(CH3CH2OH)分子中含有共价键总数为8NA | |
| C. | 1mol/LNa2CO3溶液中,含有CO32-离子数为NA | |
| D. | 6.4gCu与足量浓硝酸反应,用排水法收集的气体分子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将集有气体样品的试管倒扣于水槽中,试管中液面上升,则原气体样品中一定含NH3 | |
| B. | 将带火星的木条伸入盛满气体样品的集气瓶中,木条未复燃,则原气体样品中一定不含O2 | |
| C. | 将一定体积气体样品缓缓通入澄清石灰水中,未见有白色沉淀,则原气体样品中一定不含CO2 | |
| D. | 将一定体积气体样品缓缓通入水中,恰好完全反应生成一种盐,向所得盐溶液中加入澄清石灰水,未见沉淀生成,则原气体样品中V(NH3):V(O2)=4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在反应KC1O3+6HCl(浓)═KC1+3C12↑+3H2O中,每生成3 mol Cl2转移的电子数为NA | |
| B. | 1 mol K2S固体中含有3 NA个离子 | |
| C. | 1 mol 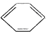 分子中含碳碳双键数为3 NA 分子中含碳碳双键数为3 NA | |
| D. | 含有NA个氖原子的氖气在标准状况下的体积约为11.2 L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
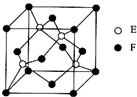 A,B,C,D,E,F是原子序数依次增大的六种前四周期元素,其相关信息如表所示:
A,B,C,D,E,F是原子序数依次增大的六种前四周期元素,其相关信息如表所示:| A | 原子半径最小的元素 |
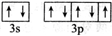
| B | 原子核外电子有6种不同的运动状态 |
| D | 原子L电子层上有2对成对电子 |
| E | E与D同主族 |
| F | 基态F+核外有3层电子且各层均处于全满状态 |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
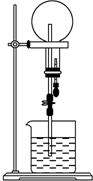 已知NH3和HCl都是能用来做喷泉实验的气体.若在同温同压下用等体积烧瓶一个收集满NH3,另一个收集HCl和N2的混合气体,如图所示.喷泉实验停止后,两个烧瓶内溶液的关系是(不考虑烧瓶内溶质的扩散,氨水的溶质按NH3计算)( )
已知NH3和HCl都是能用来做喷泉实验的气体.若在同温同压下用等体积烧瓶一个收集满NH3,另一个收集HCl和N2的混合气体,如图所示.喷泉实验停止后,两个烧瓶内溶液的关系是(不考虑烧瓶内溶质的扩散,氨水的溶质按NH3计算)( )| A. | 溶质的物质的量浓度相同、溶质的质量分数不同 | |
| B. | 溶质的质量分数相同、溶质的物质的量浓度不同 | |
| C. | 溶质的物质的量浓度和溶质的质量分数都不同 | |
| D. | 溶质的物质的量浓度和溶质的质量分数都相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60 g | B. | 66 g | C. | 90 g | D. | 184 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com