
| A��NaHCO3��Һ��Na2CO3��Һ�к��е�����������ȫ��ͬ |
| B����һ��Ũ�ȵ�NaOH��Һ�ζ�����ᣬ��pH��6ʱ����Һ��c(F��)��c(Na+)��9��9��10-7mol/L |
| C���к�ͬŨ��ͬ���������ʹ��ᣬ���ĵ�NaOH�����ʵ�������ͬ |
| D����0��2 mol/L NaOH��Һ�ζ�HCl��CH3COOH�Ļ����Һ(���Һ���������Ũ�Ⱦ�Ϊ0��1 mol/L)��������ʱ����Һ�е���δ����ȫ�к� |


 Сѧ��ʱ��ҵȫͨ����ϵ�д�
Сѧ��ʱ��ҵȫͨ����ϵ�д� �����ÿ�ʱѵ��ϵ�д�
�����ÿ�ʱѵ��ϵ�д� ��Ԫȫ��������ϵ�д�
��Ԫȫ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaHCO3��Һ�У�c(H+) + c(Na+)��c(HCO3��)+2c(CO32��) + c(OH��) |
| B��pH=12��Ba(OH)2��Һ��pH=12��Na2CO3��Һ�У�ˮ�����c(H��)һ���� |
| C��0.2mol��L��1 HCl��Һ������0.05 mol��L��1 Ba(OH)2��Һ��Ϻ���Һ��pH��1 |
| D����10 mL 0.10mol?L��1CH3COOH��Һ��������ʵ�����NaOH����Һ�����ӵ�Ũ���ɴ�С��˳���ǣ�c(Na+)��c(CH3COO��)��c(OH������c(H+) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ��
�� ��
�� ��NaOH ��
��NaOH �� ��
�� ��
�� ��
�� �����и���������ȷ����
�����и���������ȷ����| A��pH:��>��>��>�� | B�� ����>��>��>�� ����>��>��>�� |
| C����Һ��c(H��): ��>��>��>�� | D�� : ��>��>��>�� : ��>��>��>�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��W2����X+ | B��Y3+��Z2�� | C��X+��Y3+ | D��X2+��Z�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ������ | Na+��Ba2+��NH4+ | ������ | CO32����Cl����OH����SO42�� |
 = ��
= ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢� | B���ۢ� | C���� | D���ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��2C2H2(g)��5O2(g)=4CO2(g)��2H2O(l)��H����4b kJ��mol-1 |
B��C2H2(g)��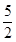 O2(g)=2CO2(g)��H2O(l)��H��2b kJ��mol-1 O2(g)=2CO2(g)��H2O(l)��H��2b kJ��mol-1 |
| C��2C2H2(g)��5O2(g)=4CO2(g)��2H2O(l)��H����2b kJ��mol-1 |
| D��2C2H2(g)��5O2(g)=4CO2(g)��2H2O(l)��H����b kJ��mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NH4Cl | B��NaOH | C��NaCl | D��H2SO4 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com