
| A.2×10-10mol/L | B.1/2(10-8+10-10)mol/L | C.(10-8+10-10)mol/L | D.1/2(10-6+10-4) |
科目:高中化学 来源:不详 题型:单选题
| A. HCl和HNO3放出H2一样多 | B.醋酸中放出H2最多 |
| C.HCl中放出H2最多 | D.HNO3比醋酸放出H2多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
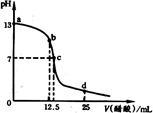
| A.若选用甲基橙指示CH3COOH滴定未知浓度的NaOH溶液的滴定终点,则测定结果偏低 |
| B.反应过程中溶液中阴、阳离子总数目:b 点大于c点 |
| C.因为CH3COONa溶液显碱性,所以当向CH3COOH溶液中加入CH3COONa时,CH3COOH电离程度将增大 |
| D.a、c区间内,c(Na+)一定大于c(CH3COO-),但c(OH-)可能大于、小于或等于c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.100℃时,pH=12的NaOH(aq)和pH=2的H2SO4(aq)恰好中和,所得溶液的pH=7 |
| B.100℃时,0.2 mol/L Ba(OH)2(aq)和0.2 mol/L HCl(aq)等体积混合,所得溶液的pH=7 |
| C.25℃时,0.2 mol/L NaOH(aq)与0.2 mol/L CH3COOH(aq)恰好中和,所得溶液的pH="7" |
| D.25℃时,pH=12的氨水和pH=2的H2SO4(aq)等体积混合,所得溶液的pH>7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.仅有② | C.②③④ | D.①②⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸式滴定管滴至终点后,俯视读数 |
| B.碱液移入锥形瓶后,加了10mL蒸馏水在滴定 |
| C.酸式滴定管用蒸馏水润洗后,未用标准液润洗 |
| D.酸式滴定管注入酸液后,尖嘴留有气泡即开始滴定,滴定终点时气泡消失 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com