
根据元素周期律,卤族元素的下列性质从上到下依次递减的有( )
|
| A. | 非金属性 | B. | 原子半径 |
|
| C. | 单质的氧化性 | D. | 氢化物的稳定性 |
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
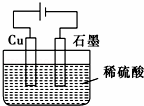
某同学按如图所示的装置进行电解实验.下列说法不正确的是( )
|
| A. | 电解过程中,铜电极上有H2产生 |
|
| B. | 电解初期,总反应方程式为Cu+H2SO4 |
|
| C. | 电解一定时间后,石墨电极上有铜析出 |
|
| D. | 整个电解过程中,溶液pH值会增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一些建筑工地的食堂中,常发生将工业用盐当作食用盐而引起中毒的现象.该盐的化学式为( )
|
| A. | MgCl2 | B. | KCl | C. | NaNO2 | D. | MgSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列方法中,正确的是( )
|
| A. | 用湿润的红色石蕊试纸检验氨气 |
|
| B. | 在样品溶液中先加入硝酸银溶液,再加入稀硝酸,若白色沉淀存在,则样品中含有Cl﹣ |
|
| C. | 将熟石灰和氯化铵混合加热,可以制备氨气 |
|
| D. | 加热试管中的氯化铵固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醛分子式为CH2O,有强烈刺激性气味的气体,甲醛在常温下是气态,被世界卫生组织确定为致癌和致畸形物质.下列关于其结构及性质的分析正确的是( )
|
| A. | C原子采取sp3杂化,O原子采取sp杂化 |
|
| B. | 甲醛分子中心原子价层电子对数为4,含有一对孤电子对,是三角锥形结构 |
|
| C. | 甲醛分子与水分子间可以形成氢键,甲醛分子间不能形成氢键 |
|
| D. | 甲醛分子为非极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
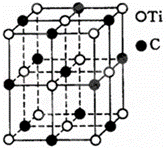
一种由钛(Ti)原子和碳原子构成的气态团簇分子,分子模型如图所示,其中圆圈表示钛原子,黑点表示碳原子,则它的化学式为( )
|
| A. | TiC | B. | Ti13C14 | C. | Ti4C7 | D. | Ti14C13 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某配位化合物的水溶液为深蓝色,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l2:4:4:1:1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n1)d n+6nsl,回答下列问题。
(1)元素D在周期表中的位置是 。
(2)该配位化合物的化学式为 。
 (3)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,两种化合物可任意比互溶,解释其主要原因为 。
(3)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,两种化合物可任意比互溶,解释其主要原因为 。
(4)A元素与B元素可形成分子式为A2B2的某化合物,该化合物的分子具有平面结构,则其结构式为 。
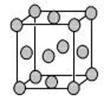
(5)已知E的晶胞结构如图所示,则E的配位数 ;EDC4常作电镀液,其中DC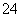 的空间构型是 ,其中D原子的杂化轨道类型是 。
的空间构型是 ,其中D原子的杂化轨道类型是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com