

| A.在相同条件下随着卤素原子核电荷数的增加,平衡时X2的转化率逐渐降低 |
| B.t2>t1,HX的生成反应是吸热反应 |
| C.随着卤素原子核电荷数的增加HX的还原性逐渐减弱 |
| D.随着卤素原子核电荷数的增加HX的稳定性逐渐增强 |
科目:高中化学 来源:不详 题型:单选题
| A.25°C时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 |
| B.25°C时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大 |
| C.25°C时Mg(OH)2固体在20 mL 0.01 mol/L氨水中的Ksp比在20mL 0.01mol/L NH4Cl溶液中的Ksp小 |
| D.25°C时,在Mg(OH)2的悬浊液加入NaF溶液后,Mg(OH)2不可能转化成为MgF2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
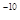 、5.0×10
、5.0×10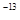 、8.3×10
、8.3×10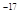 。下列有关说法错误的是 ( )
。下列有关说法错误的是 ( )| A.常温下在水中溶解能力AgCl>AgBr>Agl |
| B.在AgCl饱和液中加入足量浓NaBr溶液有AgBr沉淀生成 |
| C.在AgBr饱和溶液中加入足量浓NaCl溶液不可能有AgCI沉淀生成 |
| D.在AgI饱和液中加入NaI固体有AgI沉淀析出 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
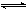 Ca2++2OH-
Ca2++2OH-| A.溶液中Ca2+数目增多 | B.溶液中Ca2+数目不变 |
| C.c(Ca2+)增大 | D.c(Ca2+)不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
A.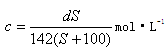 | B.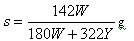 |
| C.100X=YS | D.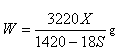 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶度积小的沉淀可以转化为溶度积更小的沉淀 |
| B.若先加入Na2S溶液,再加入KI溶液,则无黄色沉淀产生 |
| C.25℃时,饱和AgCl、AgI、Ag2S溶液中所含Ag+的浓度相同 |
| D.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解度不同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
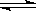 Ag+ + Cl-,现将足量的氯化银分别放入下列选项的溶液中,充分搅拌后,相同温度下,银离子浓度最小的是( )
Ag+ + Cl-,现将足量的氯化银分别放入下列选项的溶液中,充分搅拌后,相同温度下,银离子浓度最小的是( )| A.100mL蒸馏水中 | B.50mL0.1mol?L-1的氯化镁溶液 |
| C.150mL0.1mol?L-1的氯化钠溶液 | D.50mL0.1mol?L-1的氯化铝溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com