
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得到下图,则曲线a、b、c、d所对应的实验组别可能是( )
| 组别 | c(HCl)(mol·L-1) | 温度(℃) | 状态 |
| 1 | 2.0 | 25 | 块状 |
| 2 | 2.5 | 30 | 块状 |
| 3 | 2.5 | 50 | 块状 |
| 4 | 2.5 | 50 | 粉末状 |
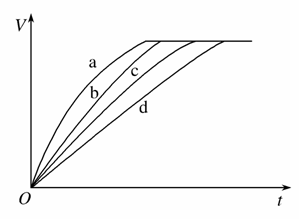
A.4-3-2-1 B.1-2-3-4
C.3-4-2-1 D.1-2-4-3
 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案科目:高中化学 来源: 题型:
对维生素的下列说法中不正确的是( )
|
| A. | 维生素是参与生物生长发育与新陈代谢所必需的一类小分子化合物 |
|
| B. | 根据溶解性的不同维生素可分为脂溶性和水溶性维生素 |
|
| C. | 维生素是参与生物生长发育与新陈代谢所必需的一类高分子化合物 |
|
| D. | 脂溶性维生素与脂类食物共食更有利于吸收 |
查看答案和解析>>
科目:高中化学 来源: 题型:
请根据实验内容,回答问题:
(1)实验室制取乙炔的反应方程式为 ,为除去乙炔中的H2S、PH3,把生成的气体通入 溶液中(填化学式),把乙炔通入溴水中,现象为 ,所得有机产物的名称为 .
(2)含有杂质的工业乙醇的蒸馏装置中,玻璃仪器有酒精灯、蒸馏烧瓶、 、 、牛角管、锥形瓶.
(3)除去苯甲酸晶体中的不溶性杂质,实验步骤为:加热溶解,蒸发浓缩, , ,过滤, ,干燥.
(4)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物,下列框图是分离操作步骤流程图:
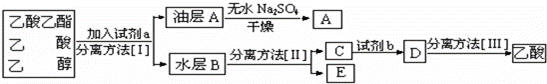
则试剂a是: ,分离方法Ⅰ是 ,分离方法Ⅱ是 ,试剂b是 ,分离方法Ⅲ是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,一定体积的密闭容器中有如下平衡:H2(g)+I2(g)2HI(g)。已知H2和I2的起始浓度均为0.10 mol·L-1,达平衡时HI的浓度为0.16 mol·L-1。则平衡时H2的浓度(mol·L-1)是( )
A.0.16 B.0.08
C.0.04 D.0.02
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应:A2+3B22AB3,以下表示的反应速率中,反应速率最快的是( )
A.v(A2)=0.4 mol·(L·min)-1
B.v(B2)=0.8 mol·(L·min)-1
C.v(AB3)=0.6 mol·(L·min)-1
D.v(A2)=0.01 mol·(L·s)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
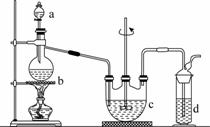
硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革还原剂。它易溶于水,不溶于醇,受热、遇酸易分解。工业上可用反应:2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2制得。实验室模拟该工业过程的装置如图所示。
回答下列问题:
(1)b中反应的离子方程式为________________,c中试剂为________。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是________。
(3)d中的试剂为________。
(4)实验中要控制SO2生成速率,可以采取的措施有___________________________________(写出两条)。
(5)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是______________________。
(6) 所得产品常含有少量Na2SO3和Na2SO4。为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀盐酸、蒸馏水中选择)
①取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,________________,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
②为减少装置C中生成Na2SO4的量,在实验过程中应注意的操作顺序是_____________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
.下列实验、现象及相关结论均正确的是( )
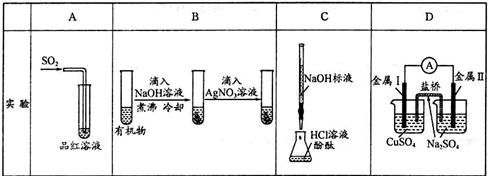
| 现象 | 品红褪色 | 最后试管有浅黄色沉淀 | 最后一滴溶液使酚酞由无色变为粉红色,且30秒不复原 | 盐桥左端从 无色逐渐变为 蓝色 |
| 结论 |
氧化性 | 有机物中含 有溴原子 | 滴定达到终点 | 金属II比I活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:
自然界的矿物、岩石的形成和变化受到许多条件的影响。地壳内每加深1 km,压强增大约25000~30000 kPa。在地壳内SiO2和HF存在以下平衡:
SiO2(s)+4HF(g)SiF4(g)+2H2O(g)
ΔH=-148.9 kJ·mol-1
如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,下列说法不正确的是( )
A.2v正(HF)=v逆(H2O)
B.v正(H2O)=2v逆(SiF4)
C.SiO2的质量保持不变
D.容器内压强不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com