
| A. | 由2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO可推出同族的硫也有Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$CuS | |
| B. | Fe3O4可表示为FeO•Fe2O3,则Pb3O4可表示为PbO•Pb2O3 | |
| C. | 氯气能把碘离子氧化为单质碘,则氯气一定能把溴离子氧化为单质溴 | |
| D. | CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2一定只生成Na2SO3和O2 |
分析 A.硫与铜反应生成硫化亚铜;
B.Pb3O4中Pb的化合价为+2、+4价;
C.氯气的氧化性强于溴与碘;
D.SO2与Na2O2发生氧化还原反应生成Na2SO4.
解答 解:A.S的氧化性较弱,与Cu反应生成Cu2S,故A错误;
B.Pb3O4中Pb的化合价为+2、+4价,不存在Pb2O3,故B错误;
C.氯气的氧化性强于溴与碘,所以氯气既能把碘离子氧化为单质碘,又能把溴离子氧化为单质溴,故C正确;
D.SO2与Na2O2发生氧化还原反应生成Na2SO4,没有氧气生成,故D错误;
故选C.
点评 本题考查常见元素化合物知识,题目难度不大,本题注意把握相关知识的积累,试题考查了学生的分析、理解能力知识迁移能力.


科目:高中化学 来源: 题型:选择题
| A. | 15mL | B. | 小于15mL | C. | 大于15mL | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述两溶液中盐酸的物质的量浓度比硫酸的物质的量浓度大 | |
| B. | 硫酸使铝钝化 | |
| C. | 生成的氯化铝能溶于水,而生成的硫酸铝难溶于水 | |
| D. | 氯离子可能破坏氧化铝薄膜,而硫酸根离子不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
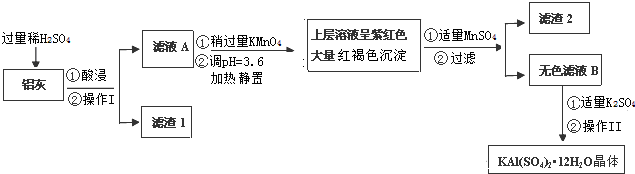
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.8 | 7.5 | 2.7 |
| 完全沉淀时 | 5.2 | 9.7 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①②③④ | C. | ②④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com