
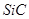 粗产品加入到过量的NaOH溶液中充分反应,收集到0.1mol氢气,过滤得SiC固体11.4g,滤液稀释到1L,生成氢气的离子方程式为,硅酸钠的物质的量浓度为
粗产品加入到过量的NaOH溶液中充分反应,收集到0.1mol氢气,过滤得SiC固体11.4g,滤液稀释到1L,生成氢气的离子方程式为,硅酸钠的物质的量浓度为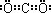 ⑵过滤,水(或乙醇)
⑵过滤,水(或乙醇)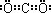 ,
,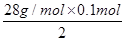 =1.4g,
=1.4g,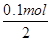 =0.05mol,
=0.05mol,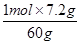 =0.12mol,
=0.12mol,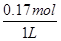 =0.17mol·L-1,
=0.17mol·L-1,

科目:高中化学 来源:不详 题型:单选题
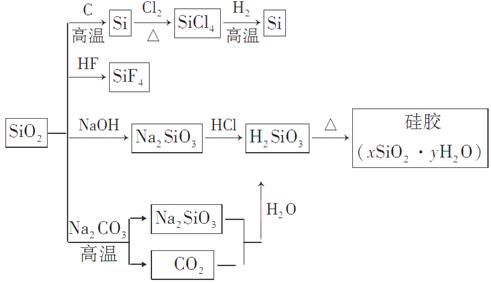
| A.SiO2属于两性氧化物 |
| B.盛放Na2CO3溶液的试剂瓶不能用玻璃塞 |
| C.硅胶吸水后不能重复再生 |
| D.图中所示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.利用Si和O在周期表中的位置 |
| B.SiO2与水不发生反应 |
| C.Si在一定条件下与氧气反应,生成SiO2 |
| D.H2SiO3的酸性比H2O的酸性强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.工业上通常以SiO2为原料,用氧化剂与其反应制备单质硅 |
| B.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一 位 |
| C.硅的化学性质不活泼,在自然界中可以以游离态存在 |
| D.硅在电子工业中,是重要的半导体材料 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.其氧化物都能与NaOH溶液反应 |
| B.其单质在加热时都能跟O2反应 |
| C.其氧化物都能溶于水生成相应的酸 |
| D.碳和硅两种元素共有两种单质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 溶液 | 操作及现象 |
| A | Ca(OH)2溶液 | 通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失。再加入足量NaOH溶液,又变浑浊。 |
| B | 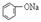 溶液 溶液 | 通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失。 |
| C | Ca(ClO)2溶液 | 通入CO2,溶液没有明显变化。再滴入品红溶液,红色褪去。 |
| D | CaCl2溶液 | 通入CO2,溶液没有明显变化。若同时通入CO2和NH3,则溶液变浑浊。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 CO(g)+H2(g) △H=+131.3kJ/mol,达到平衡后,体积不变时,能提高H2O的平衡转化率的措施是 。
CO(g)+H2(g) △H=+131.3kJ/mol,达到平衡后,体积不变时,能提高H2O的平衡转化率的措施是 。| A.升高温度 | B.增加碳的用量 |
| C.加入催化剂 | D.用CO吸收剂除去CO |
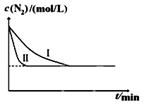
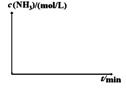
 CO2(g)+H2(g)得到如下数据:
CO2(g)+H2(g)得到如下数据:| 温度/℃ | 起始浓度mol/L | 平衡浓度mol/L | |
| CO(g) | H2O(g) | H2(g) | |
| 900 | 2.0 | 0.8 | 0.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com