
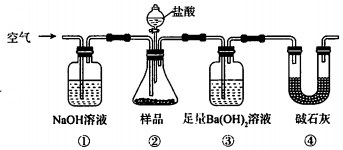
| A. | 必须在②③间添加吸收HCl的装置 | |
| B. | ④的作用是防止空气中的气体影响实验的精确度 | |
| C. | 通入空气的作用是保证②中产生的气体完全转移到③中 | |
| D. | 称取样品和③中产生的沉淀的质量即可求算Na2CO3固体的纯度 |
分析 测定Na2CO3固体(含少量NaCl)的纯度,用应先通入空气,氢氧化钠溶液用于除去空气中的二氧化碳,盐酸和样品反应生成二氧化碳,氢氧化钡与二氧化碳反应生成碳酸钡沉淀,根据沉淀的质量可确定二氧化碳的质量,进而计算碳酸钠的质量,可计算样品的含量,装置中碱石灰可用于吸收空气中的二氧化碳,减少实验误差,以此解答该题.
解答 解:A.氢氧化钡足量,可与氯化氢反应,同时吸收二氧化碳,无需单独添加吸收HCl的装置,故A错误;
B.碱石灰可与二氧化碳反应,可防止空气中的气体影响实验的精确度,故B正确;
C.通入空气,可将生成的二氧化碳完全转移到③中,以被充分吸收,减小实验误差,故C正确;
D.③中产生的沉淀为碳酸钡,根据碳酸钡的质量可计算样品中的碳酸钠,可计算样品含量,故D正确.
故选A.
点评 本题考查物质的含量的测定,为高频考点,侧重考查学生的分析能力和实验能力,注意把握物质的性质以及实验的原理,把握操作方法,难度不大.


科目:高中化学 来源: 题型:解答题
 如图所示,U形管内盛有100mL的溶液,按要求回答下列问题:
如图所示,U形管内盛有100mL的溶液,按要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图X为电源,椭圆形滤纸Y浸透饱和食盐水和酚酞试液,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向c端扩散.下列判断正确的是( )
如图X为电源,椭圆形滤纸Y浸透饱和食盐水和酚酞试液,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向c端扩散.下列判断正确的是( )| A. | b为电源的正极,d点周围变红 | B. | Cu电极质量减小,Pt电极质量增大 | ||
| C. | Z中溶液的pH先减小,后增大 | D. | 溶液中的SO42-向Pt电极定向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF的熔、沸点比ⅦA族其他元素氢化物的高 | |
| B. | 水分子高温下也很稳定 | |
| C. | 冰的密度比液态水的密度小 | |
| D. | NH3极易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
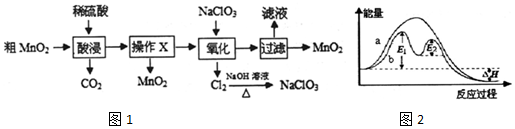
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W>Y>Z>X | |
| B. | 2.24 L(标准状况)M溶于1 L水中,所得溶液的pH约为13 | |
| C. | YZ2能使湿润的淀粉KI试纸变蓝 | |
| D. | Y、W的最髙价氧化物对应的水化物均为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢是原子半径最小的元素 | |
| B. | 氟是非金属性最强的元素 | |
| C. | 硅元素适合作半导体材料 | |
| D. | 稀有气体元素原子的最外层电子数均为8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com