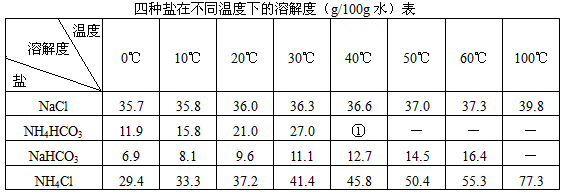
根据侯德榜制减法原理并参考下表的数据,实验室制备纯碱Na2CO2的主要步骤是:将配制好的饱和NaCl溶液倒入烧杯中加热,控制温度在30-35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕后,继续保温30分钟,静置、过滤得NaHCO3晶体。用少量蒸馏水洗涤除去杂质,抽干后,转入蒸发皿中,灼烧2小时,制得Na2CO3固体。
①>35°NH4HCO3会有分解
请回答:
(1)反应温度控制在30-35℃,是因为若高于35℃则 ,若低于30℃,则________________________;为控制此温度范围,采取的加热方法为________________________。
(2)加料完毕后,继续保温30分钟,目的是________________________。静置后只析出NaHCO3晶体的原因是________________________。用蒸馏水洗涤NaHCO3晶体的目的是除去___________________杂质(以化学式表示)。
(3)过滤所得的母液中含有____________(以化学式表示),需加入________________,并作进一步处理,使NaCl溶液循环使用,同时可回收NH4Cl。
(4)测试纯碱产品中NaHCO3含量的方法是:准确称取纯碱样品Wg,放入锥形瓶中加蒸馏水溶解,加
1-2滴酚酞指示剂,用物质的量浓度为c(mol/L)的HCl溶液滴定至溶液由红色到无色(指示CO32-+H+=
HCO3-反应的终点),所用HCl溶液体积为V1mL,再加1-2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所HCl溶液总体积为V2mL。写出纯碱样品中NaHCO3质量分数的计算式:NaHCO3(%)=
____________。

 名校课堂系列答案
名校课堂系列答案