
某氢氧燃料电池的电解液是热的KOH溶液,在正极上氧气被还原,在负极上氢气被氧化,下列有关该电池的叙述正确的是
A.负极反应式为:H2+2OH- -2e- =2H2O
B.正极反应式为:O2 +4H+十4e- =2H2O
C.工作一段时间后,KOH溶液的浓度不变
D.电池工作时,电子由正极通过外电路流向负极
科目:高中化学 来源:2013-2014福建省福州八县第二学期期中考试高一化学试卷(解析版) 题型:填空题
短周期元素X、Y、Z、W 的原子序数依次增大, X 的原子半径比Y 的小,X 与W 同主族,Z 是地壳中含量最高的元素.X、Y、Z、W 原子最外层电子数之和为13。问:
(1)X是 Y是 Z是 W是 (填元素符号)
(2)写出W的最高价氧化物对应的水化物的电子式
写出Y的简单氢化物的电子式
(3)Y的最高价氧化物对应的水化物的浓溶液久置后呈现黄色,写出发生反应的化学方程式
(4)实验室制取Y的氢化物的化学方程式:_______________________________,该反应________(填“是”或“不是”)氧化还原反应。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省漳州市八校高三第四次联考理综化学试卷(解析版) 题型:实验题
(15分)实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),过程如下:
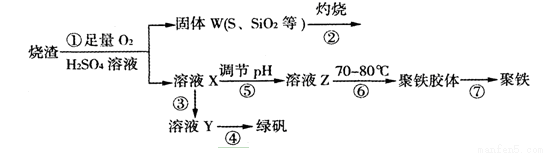
(1)将过程②中的产生的气体通入下列溶液中,溶液会褪色的是 ;
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.溴水
(2)过程①中,FeS和O2、H2SO4反应的离子方程式为: ;
(3)过程③中,需加入的物质是 ;
(4)过程④中,蒸发结晶需要使用酒精灯、三角架、泥三角,还需要的仪器有 ;
(5)过程⑤调节pH可选用下列试剂中的 (填选项序号);
A.稀硫酸 B.CaCO3 C.NaOH溶液
(6)过程⑥中,将溶液Z加热到70一80℃,目的是 ;
(7)实验室为测量所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取2.700g样品;②将样品溶于足量的盐酸后,加入过量的氯化钡溶液;③过滤、洗涤、干燥,称量,得固体质量为3.495g。若该聚铁主要成分为[(Fe(OH)(SO4)]n,则该聚铁样品中铁元素的质量分数为 。(假设杂质中不含铁元素和硫元素)。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高二下学期期末考试化学试卷(解析版) 题型:选择题
25 ℃在等体积的①pH=0的H2SO4溶液,②0.05 mol·L-1的Ba(OH)2溶液,③pH = 10的Na2S溶液,④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是( )
A.1∶10∶1010∶109 B.1∶5∶5×109∶5×109
C.1∶20∶1010∶109 D.1∶10 ∶104∶109
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高二下学期期末考试化学试卷(解析版) 题型:选择题
在容积可变的密闭容器中,1molN2和4molH2在一定条件下发生反应,达到平衡时,H2的转化率为25%,则平衡时的氮气的体积分数接近于
A.5% B.10% C.15% D.20%
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高二下学期期末考试化学试卷(解析版) 题型:选择题
已知:2H2(g)+O2(g)=2H2O(g);ΔH=-270kJ·mol-1,下列说法错误的是
A.2mol水蒸气分解成2mol氢气与1mol氧气吸收270kJ热量
B.2mol氢气与1mol氧气反应生成2mol液态水放出热量大于270kJ
C.在相同条件下,2mol氢气与1mol氧气的能量总和大于2mol水蒸汽的能量
D.2个氢气分子与1个氧气分子反应生成2个水蒸汽分子放出270kJ热量
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省宁德市高三5月质检理综化学试卷(解析版) 题型:选择题
W、X、Y、Z四种短周期元素。已知X原子的核外电子数和Ne原子相差1,在同周期中X原子半径最大,W、Y、Z在周期表中的相对位置如图,Z的非金属性在同周期元素中最强。下列说法不正确的是

A.简单离子半径:Y>X
B.最高价氧化物对应水化物的酸性:Z>Y
C.W与X形成的化合物属于离子化合物
D.W、X、Z只能形成一种化合物
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高三热身考试化学试卷(解析版) 题型:填空题
[化学—有机化学基础](13分)
某研究小组以甲苯为主要原料,采用以下路线合成医药中间体F和Y。
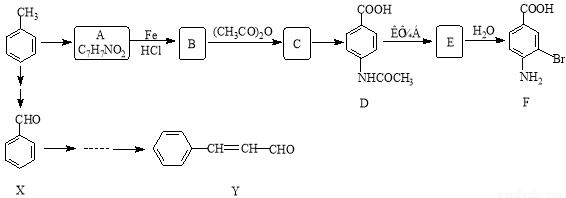
已知: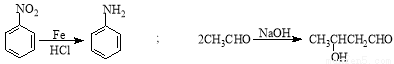 。
。
请回答下列问题:
(1)写出Y中含氧官能团的名称 。
(2)下列有关F的说法正确的是 。
A.分子式是C7H7NO2BrB.既能与盐酸反应又能与NaOH溶液反应
C.能发生酯化反应 D.1 mol F最多可以消耗2 mol NaOH
(3)写出由甲苯→A反应的化学方程式 。
(4)在合成F的过程中,B→C步骤不能省略,理由是 ;
F在一定条件下形成的高分子化合物的结构简式是 。
(5)写出一种同时符合下列条件的Y的同分异构体的结构简式 。
①苯环上只有两种不同化学环境的氢原子②与足量浓溴水反应产生白色沉淀
③分子中只存在一个环状结构
(6)以X和乙烯为原料可合成Y,依次指出三步合成过程中三个主要反应的反应类型:
、 、 。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高二下学期期末考试化学试卷(解析版) 题型:选择题
在前一种分散系中慢慢滴加后一种试剂,能观察到先有沉淀生成后变澄清的是
①氯化铝溶液中滴加氢氧化钠溶液
②偏铝酸钠溶液中滴加盐酸
③氢氧化钠溶液中滴加氯化铝溶液
④蛋白质溶液中滴加硫酸铜溶液
⑤氯化铝溶液中滴加氨水
⑥硝酸银溶液中滴加氨水
⑦氢氧化铁胶体中滴加硫酸
A. ①②⑥⑦ B.②③⑤⑦ C. ①②④⑥ D.③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com