
| | | | |||||||||||||||
| | | | | | | A | | | |||||||||
| | B | C | | | D | E | | ||||||||||
| | | | | | | | | | | | | | | | | | |
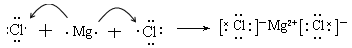
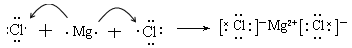 。
。

科目:高中化学 来源:不详 题型:单选题
| A.第1列元素均能形成M2O和M2O2型化合物 |
| B.第14列元素所形成的化合物种类最多 |
| C.第17列元素均有最高价氧化物R2O7 |
| D.最外层有两个电子的原子都在第2列 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 族 周期 | IA | IIA | IIIA | VIA | VA | VIA | VIIA | 0 |
| 2 | | | | ⑥ | | ⑦ | | |
| 3 | ① | ③ | ⑤ | | | | ⑧ | ⑩ |
| 4 | ② | ④ | | | | | ⑨ | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素原子的核外电子排布呈周期性变化 | B.元素原子的电子层数呈周期性变化 |
| C.元素的化合价呈周期性变化 | D.元素原子半径呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③ | B.②④ | C.①④ | D.②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
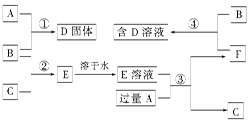
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com