
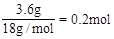 ������0.4molH��
������0.4molH��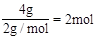 ��11.2LO2�����ʵ���Ϊ
��11.2LO2�����ʵ���Ϊ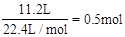 ������Ϊ16g��1molH2O������Ϊ18g����˺�������������H2������������H2O��
������Ϊ16g��1molH2O������Ϊ18g����˺�������������H2������������H2O��

 �����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����״���£�22.4L����Ȼ�ϵ�H2��CO2�������к��еķ���������ΪNA |
| B��ˮ��Ħ����������NA��ˮ���ӵ���Է�������֮�� |
| C����״���£�5.6L���Ȼ�̼���еķ�����Ϊ0.25NA |
| D���ֱ���NA��ˮ������ɵı���ˮ��ˮ����������������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
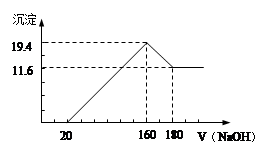
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1L H2SO4��Һ�к���98g H2SO4�������Һ�����ʵ���Ũ��Ϊ98g/L |
| B��1LH2O���ܽ���0.5molNaCl�������Һ�����ʵ���Ũ��Ϊ0.5mol/L |
| C����1L 1mol/L ������Һ��ȡ��100mL��Һ�������ʵ���Ũ����Ϊ1mol/L |
| D��0.5mol/L ��NaOH��Һ�У�����0.5mol Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������Ħ���������22.4L/mol |
| B���ڱ�״���£�1mol�κ�������ռ���������22.4L/mol |
| C���ڱ�״���£�1mol�κ�������ռ�������Լ��22.4L |
| D���ڱ�״���£�1molˮ��ռ�����ԼΪ22.4L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��23g�����Ʊ�Ϊ������ʱʧȥ�ĵ�����ΪNA |
| B��12 g C-13���е�ԭ����ΪNA�� |
| C����״���£�22.4 L����������ԭ����ĿΪ2NA |
| D�����³�ѹ�£�28g N2��CO�Ļ����������ԭ����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��10mL 1mol/L (NH4)2SO4��Һ | B��50mL 0.2mol/L NH4Cl��Һ |
| C��10mL 0.2mol/L(NH4)2SO4��Һ | D��200mL 0.1mol/L NH4NO3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ά��ˮ�������ˮ��õ������ղ��ﲻͬ |
| B��3.36L��ϩ�к��еĹ��õ��Ӷ���Ϊ1.5NA |
| C���Թ�������������ۣ��ټ���һ����ϡ���ᣬ����3��4���ӣ�Ȼ�����������Һ��Ƭ�̺�ܱ����С����������� |
| D������Ƥ�����Ҫ�ɷ��ǵ����ʣ�����Ȼ������ˮ������ղ����ǰ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��2�� | B��3�� | C��4�� | D��5�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com