
(13分)硫代硫酸钠(Na2S2O3)俗称海波,它可看成是用一个S原子取代了Na2SO4中的一个O原子而形成的。某校化学研究性学习小组用类比学习思想,并通过实验探究Na2S2O3的化学性质。
【提出问题】Na2S2O3与Na2SO4结构相似,化学性质是否也相似呢?
【实验探究】取适量Na2S2O3晶体,溶于水制成Na2S2O3溶液,进行如表所示的探究,完成表中有关内容。
实验操作 | 实验现象 | 现象解释(用离子方程式表示) |
探究①A. B.向pH=2的硫酸中滴加Na2S2O3溶液 | a.溶液pH=8 b. | i. ii. S2O32-+2H |
探究②C.向新制氯水(pH<2)中滴加少量Na2S2O3溶液 | c.氯水颜色变浅 | iii. |
【实验结论】探究① 探究② 。
根据探究①和探究②的结论,Na2S2O3和Na2SO4化学性质 。
【问题讨论】
(1)甲同学向探究②反应后的溶液中滴加AgNO3溶液,出现白色沉淀,据此甲同学认为氯水可将Na2S2O3氧化。你认为此方案是否正确并说明理由: 。
(2)请你重新设计一个实验方案,证明Na2S2O3能被氯水氧化。你设计的方案是 。
A.用玻璃棒蘸取Na2S2O3溶液点在pH试纸上,并与标准比色卡对照(1分)
i. S2O32-+H2O HS2O3-+OH-(2分)
HS2O3-+OH-(2分)
B. 有淡黄色沉淀(1分),有无色刺液性气味气体产生(1分)
iii. S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+(2分)
探究①:Na2S2O3溶液呈碱性(1分),能与强酸反应(1分)。
探究②:Na2S2O3具有还原性(1分),不相似(1分)。
【问题与讨论】(1)不正确,因为氯水中含有Cl-(1分)。
(2)取少量探究②反应后的溶液,向其中滴入BaCl2溶液,若有白色沉淀,则说明Na2S2O3被氯水氧化。(1分)
【解析】
试题分析:A.根据实验现象可知,该步操作是测定溶液pH值的,因此正确的操作应该是用玻璃棒蘸取Na2S2O3溶液点在pH试纸上,并与标准比色卡对照。
i.溶液显碱性,说明酸根水解,离子方程式为S2O32-+H2O HS2O3-+OH-。
HS2O3-+OH-。
B.根据反应的生成物有单质硫和 二氧化硫生成可知,实验现象为有淡黄色沉淀,有无色刺液性气味气体产生。
iii.氯水颜色变浅说明发生了氧化还原反应,即硫代硫酸钠被氧化,则反应的离子方程式为S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+。
根据实验操作以及实验现象可知探究①是探究Na2S2O3溶液呈碱性,能与强酸反应。探究②是探究Na2S2O3具有还原性。由于硫酸钠不能与强酸反应,也没有还原性,所以二者的性质不相似。
【问题与讨论】(1)因为氯水中含有Cl-也能与硝酸银溶液反应产生白色沉淀,因此结论是不正确的。
(2)由于氧化产物是硫酸钠,因此可以通过验证硫酸根的生成即可,则实验操作为取少量探究②反应后的溶液,向其中滴入BaCl2溶液,若有白色沉淀,则说明Na2S2O3被氯水氧化。
考点:考查实验方案设计与探究


科目:高中化学 来源:2013-2014四川省成都市高第二期期末高一化学试卷(解析版) 题型:选择题
下列化学用语正确的是 ( )
A. CH3COOH的球棍模型
B.第三周期简单阴离子结构示意图均可表示为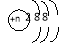
C.HIO结构式为 H-I-O
D. 37Cl 中的37代表该原子的相对原子质量
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省宜昌市春季期中考试高二化学试卷(解析版) 题型:填空题
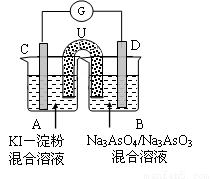
(12分)(1)右图为阳离子交换膜法电解饱和食盐水(滴有酚酞)原理示意图,E口产生H2,电解食盐水的离子方程式为: ,溶液变红色的是: 区(填A或B)。
(2)电化腐蚀是钢铁发生腐蚀的主要原因,又可分为吸氧腐蚀和析氢腐蚀,发生吸氧腐蚀的电极反应式:负极 正极
(3)下图是一套电化学实验装置,图中C、D均为铂电极,U为盐桥,G是灵敏电流计
此装置中进行的反应是可逆反应,其反应方程式式为:AsO43-+2I-+H+ AsO33-+I2+H2O,向B杯中加入适量较浓的硫酸,发现G的指针向右偏移。此时A杯中的主要实验现象是 D电极上的电极反应式为
AsO33-+I2+H2O,向B杯中加入适量较浓的硫酸,发现G的指针向右偏移。此时A杯中的主要实验现象是 D电极上的电极反应式为
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省宜昌市春季期中考试高二化学试卷(解析版) 题型:选择题
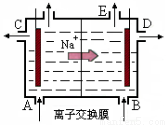
在密闭容器中,对于可逆反应A+3B 2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
A.若正反应方向ΔH<0,则T1>T2
B.压强增大时,混合气体的平均相对分子质量减小
C.B一定为气体
D.A一定为气体
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省宜昌市春季期中考试高二化学试卷(解析版) 题型:选择题
某混合溶液中所含离子的浓度如下表,则M离子可能为
所含离子 | NO3- | SO42- | H+ | M |
浓度 /(mol·L-1) | 2 | 1 | 2 | 1 |
A.Cl- B.Ba2+ C.Na+ D.Mg2+
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省高三5月冲刺卷理综化学试卷(解析版) 题型:选择题
下列解释实验事实的化学方程式正确的是
A.5molFe和4molCl2反应:5Cl2+4Fe点燃2FeCl2+2FeCl3
B.2molKMnO4和3molH2O2在酸性条件下反应:2MnO4-+3H2O2+6H+=Mn2++4O2↑+6H2O
C.在电解液为氢氧化钾的甲醇燃料电池内电路中,阳极的电极反应式为:CH3OH-6e-+8OH-=CO32-+6H2O
D.向NaAlO2溶液中通入过量CO2:CO2+3H2O+2AlO2-=2Al(OH)3↓+CO32-
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:填空题
(14分)已知:A为含金属离子的淡黄色固体化台物,E、X为空气中常见气体,A、B、C、D含有相同的金属离子,其转化关系如下图(部分产物已略去)。
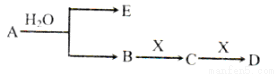
请回答下列问题
(1)这种金属离子的离子结构示意图为_____________;
(2)X的电子式_______________;
(3)B中所含化学键的类型是_____________;
常温常压下,7.8gA与足量的水充分反应放出热量a kJ,写出该反应的热化学方程式
_________________________________________________________________.
(4)①C也可转化为B,写出该转化的化学方程式_______________________________;
②B与D反应的离子方程式为_______________________________________.
(5)将一定量的气体X通入2LB的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。
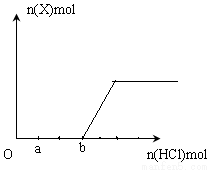
请回答:a点溶液中所含溶质的化学式为__________ ,a-b之间的反应的离子方程式是_________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省长春市高二下学期期末考试化学试卷(解析版) 题型:选择题
在A2+3B2 = 2C的反应中,经过t秒钟后,C的浓度增加了0.6mol/L,在此期间,反应速率V(B2)=0.45mol/(L·S),则t值为
A.1秒 B.1.5秒 C.2秒 D.2.5秒
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省白城市高二上学期期末考试化学(B卷)试卷(解析版) 题型:选择题
下列叙述正确的是
A.在原电池的正极和电解池的阳极上发生的都是氧化反应
B.实验室用惰性电极电解NaCl溶液,阴、阳两极收集到的气体体积之比为2∶1
C.用铜作电极电解稀硫酸,可能发生反应:Cu+H2SO4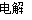 CuSO4+H2↑
CuSO4+H2↑
D.在用惰性电极电解稀硫酸的过程中,溶液pH保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com