
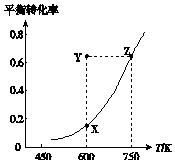
 甲醇脱氢可制取甲醛CH3OH(g)?HCHO(g)+H2(g)△H,甲醇的平衡转化率随温度变化的曲线如图所示.下列有关说法正确的是( )
甲醇脱氢可制取甲醛CH3OH(g)?HCHO(g)+H2(g)△H,甲醇的平衡转化率随温度变化的曲线如图所示.下列有关说法正确的是( )| A. | △H<0 | B. | 从Y点到Z点可通过升高温度实现 | ||
| C. | 从Y点到X点可通过使用催化剂实现 | D. | 600 K时,Y点甲醇的v正<v逆 |
分析 A、甲醇脱氢反应为吸热反应还是放热反应由温度对平衡移动的影响确定;
B、升高温度,平衡向正反应方向移动,甲醇转化率增大;
C、使用催化剂平衡不移动;
D、600K时Y点甲醇转化率大于X点甲醇平衡转化率.
解答 解:A、由图可知,温度越高甲醇平衡转化率越大,说明升高温度化学平衡正向移动,因此甲醇脱氢反应为吸热反应即△H>0,故A错误;
B、由图可知Y点和Z点甲醇转化率相等,升高温度,平衡向正反应方向移动,则甲醇转化率增大,所以从Y点到Z点不能通过升高温度实现,故B错误;
C、Y点和X点两点甲醇的平衡转化率不同,如果从Y点到X点平衡发生移动,所以不是使用催化剂,故C错误;
D、600K时Y点甲醇转化率大于X点甲醇平衡转化率,说明反应逆向进行即:υ(正)<υ(逆),故D正确.
故选:D.
点评 本题考查化学平衡影响因素、焓变判断等,从图中提取有用信息的能力尤为关键,难度中等,注意基础知识理解掌握.


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:填空题
| A组物质 | 熔点/K | B组物质 | 熔点/K |
| NaCl | 1 074 | Na | 317 |
| KCl | 1 049 | Mg | 923 |
| CsCl | 918 | Al | 933 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
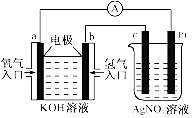 由化学能转变的热能或电能仍然是人类使用的主要能源.根据如图所示的装置,判断下列说法不正确的是( )
由化学能转变的热能或电能仍然是人类使用的主要能源.根据如图所示的装置,判断下列说法不正确的是( )| A. | 该装置中Pt极为阳极 | |
| B. | 当c极的质量变化了2.16g时,a极上消耗的O2在标准状况下的体积为1.12L | |
| C. | 该装置中b极的电极反应式是:H2+2OH--2e-=2H2O | |
| D. | 该装置中a极为正极,发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使红色石蕊试纸变蓝的溶液中:Na+、K+、NO3-、AlO2- | |
| B. | 在含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| C. | 在加入铝粉能产生氢气的溶液中:NH4+、Fe2+、SO42-、NO3- | |
| D. | 能使湿润的淀粉碘化钾试纸变蓝的溶液中:Na+、NH4+、S2-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用丁达尔效应区分氢氧化铁胶体与氯化铜溶液 | |
| B. | 用澄清石灰水鉴别NaHCO3和Na2CO3 | |
| C. | 用分液法分离植物油和水的混合物 | |
| D. | 用淀粉溶液检验食盐溶液中是否存在I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电子由石墨电极流向银电极 | |
| B. | 多孔石墨电极上发生发生氧化反应 | |
| C. | 正极的电极反应式方程式为:2Ag++I2+2e -═2AgI | |
| D. | 当电池中有1 mol e一转移时消耗02的体积5.6 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com