
【题目】下列说法不正确的是 ( )
A. 阿司匹林具有解热镇痛作用
B. 长期饮用纯净水,有可能引起一些微量元素缺乏症
C. Al(OH)3能用于治疗胃酸过多
D. 使用青霉素时,直接静脉注射可以不用进行皮肤敏感测试
科目:高中化学 来源: 题型:
【题目】金刚石与石墨是碳的两种同素异形体,在100kPa时,1mol石墨转化为金刚石要吸收1.895kJ的热量,下列说法正确的是( )
①金刚石比石墨稳定
②石墨比金刚石稳定
③1mol石墨比1mol金刚石的总能量高
④1mol石墨比1mol金刚石的总能量低
A.②③B.①③C.②④D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要配制0.50mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.
(1)选择仪器.完成本实验所必需的仪器有:托盘天平(精确到0.1g)、药匙、烧杯、玻璃棒、、以及等质量的两片滤纸.
(2)计算.配制该溶液需取NaCl晶体g.
(3)称量.①天平调平之后,应将天平的游码调至某个位置,请在图1中用一根竖线标出游码左边缘所处的位置: 
②称量过程中NaCl晶体应放于天平的(填“左盘”或“右盘”).
③称量完毕,将药品倒入烧杯中.
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是 .
(5)转移、洗涤.在转移时应使用引流,需要洗涤烧杯2~3次是为了 .
(6)定容,摇匀. 将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配制的时间、、 .
(7)在配制过程中,某学生观察定容时液面情况如图2所示,所配溶液的浓度会(填“偏高”、“偏低”或“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摩尔质量是指单位物质的量的物质所具有的质量.
(1)已知O的相对原子质量为16,则O3的摩尔质量为 .
(2)48gN2H4的物质的量为 , 所含氢原子数目为 .
(3)标准状况下,相同体积的CH4和SO2气体的质量比为;相同质量的CH4和SO2分子个数比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法错误的是 ( )
A. 硅可用于制造光导纤维 B. 铝槽车可用于浓硫酸的贮运
C. 铝热反应可用于焊接铁轨 D. 呈液态的钠钾合金可用于原子反应堆的热交换剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以废旧锌锰电池初步处理分选出的含锰废料(MnO2、MnOOH、MnO及少量Fe、Pb等)为原料制备高纯MnCl2·xH2O,实现锰的再生利用。其工作流程如下:
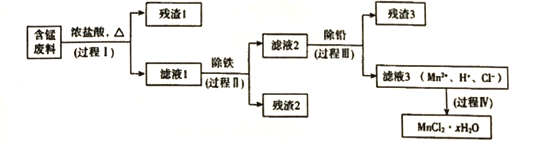
资料a: Mn的金属活动性强于Fe;Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
资料b:生成氢氧化物沉淀的pH见下表(金属离子的起始浓度为0.1 mol·L-1)
Mn(OH)2 | Pb(OH)2 | Fe(OH)3 | |
开始沉淀时 | 8.1 | 6.5 | 1.9 |
完全沉淀时 | 10.1 | 8.5 | 3.2 |
(1)过程I的目的是浸出锰。经检验滤液1中含有的阳离子为Mn2+、Fe3+、Pb2+和H+。
①MnO2与浓盐酸反应的离子方程式是__________________________________。
②检验滤液1中只含Fe3+不含Fe2+的操作和现象是:取少量滤液1于试管中,滴入黄色K3[Fe(CN)6](铁氰化钾)溶液,无明显变化:另取少量滤液1于试管中,___________________________。
③Fe3+由Fe2+转化而成,可能发生的反应有:i.2Fe2++Cl2=2Fe3++2Cl-
ii.4Fe2++O2+4H+=4Fe3++2H2O iii.……
写出iii的离子方程式:___________________________。
(2)过程II的目的是除铁,有如下两种方法:
i.氨水法:将滤液1先稀释,再加适量10%的氨水,过滤。
ii.焙烧法:将滤液1浓缩得到的固体于290°C焙烧,冷却,取焙烧物……
己知:焙烧中发生的主要反应2FeCl3+3O2=2Fe2O3+3Cl2,焙烧时MnCl2和PbCl2不发生变化。
①氨水法除铁时,溶液pH应控制在 _______________之间。
②补全ii中的操作:____________________。
③两种方法比较,氨水法除铁的缺点是_________________________________________。
(3)过程III的目的是除铅。加入的试剂是______________________。
(4)过程IV所得固体中的x的测定如下:取m1g样品,置于氮气氛围中加热至失去全部结晶水时,质量变为m2g。则x=________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列符合未来新能源标准的是( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④B.⑤⑥⑦⑧
C.①⑤⑥⑦⑧D.③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O盐桥中装有饱和K2SO4溶液,下列叙述中正确的是( )
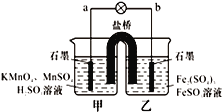
A. 外电路的电流方向是从a到b
B. 甲烧杯中溶液的pH逐渐减小
C. 电池工作时,盐桥中的SO42-移向甲烧杯
D. 乙烧杯中发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
实验室以有机物 A、E 为原料,制备聚酯纤维 M 和药物中间体 N 的一种合成路线如下:

已知: ①A 的核磁共振氢谱有 3 组峰
②
③ ( R1、R2、R3、R4 表示烃基)
( R1、R2、R3、R4 表示烃基)
请回答下列问题:
(1) A 的化学名称为_________。
(2) J 的结构简式为_________。
(3) B→C、G→H 的反应类型分别为_________、_________。
(4) D+I→M 的化学方程式为_________。
(5) 同时满足下列条件的 N 的同分异构体有_________种( 不考虑立体异构), 其中任意一种的结构简式为_________。
①饱和五元碳环上连有两个取代基
②能与 NaHCO3溶液反应
③能发生银镜反应
(6) 参照上述合成路线和信息, 以环庚醇和甲醇为有机原料( 无机试剂任选), 设计制备![]() 的合成路线_____________________。
的合成路线_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com