
I.下列实验操作或对实验事实的描述中,正确的是________(填序号)。
①用量筒量取稀硫酸溶液8.0 mL;
②Fe(OH)3胶体与FeCl3溶液的混合物可用过滤的方法分离;
③用湿润的pH试纸测量某溶液pH时,测量值可能比真实值小;
④用碱式滴定管量取KMnO4溶液20.50 mL;
⑤在实验室中用锌和稀硫酸反应制氢气,为加快反应速率而不影响H2的品质,可向溶液中加适量Cu(NO3)2晶体。
Ⅱ.将某98%的浓硫酸样品敞口露置于空气中,放置24 h后,取出5 mL浓硫酸与18 mL 9 mol·L-1的NaOH溶液恰好完全中和。请回答下列问题:
(1)该硫酸样品露置24 h后,其物质的量浓度是___________mol·L-1。
(2)若分别用下列方法鉴别浓硫酸和稀硫酸,可以达到目的的是____________(填序号)。
a.常温下加入铜片 b.常温下加入铁片
c.常温下加入木炭 d.用玻璃棒各蘸取少许涂在滤纸上
(3)工业上利用过量氨水吸收硫酸工业尾气中的有害物质,请写出该过程中发生的一个反应的离子方程式_____________________________________。
科目:高中化学 来源: 题型:
对有机物 ,下列相关说法中不正确的是 ( )
,下列相关说法中不正确的是 ( )
A.一定条件下能发生酯化反应
B.一定条件下能发生催化氧化反应
C.不能发生加成反应
D.1 mol该物质与Na2CO3溶液反应最多消耗1.5 mol Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是
A.所用NaOH已吸潮
B.向容量瓶中加水时液面低于刻度线即摇匀
C.有少量NaOH溶液残留在烧杯内
D.没有洗涤烧杯和玻璃棒。
查看答案和解析>>
科目:高中化学 来源: 题型:
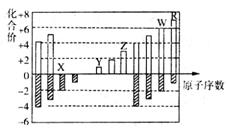
右图是部分短周期元素化合价与原子序数的关系图(X、Y、Z、W、R代表元素符号)下列说法中,正确的是
A.原子半径比较:Z的>Y的>X的
B.气态氢化物的还原性比较:W的>R的
C.WX3和水反应形成的化合物是离子化合物
D.含Z元素的盐溶液一定显示酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与人类生活密切相关。下列说法正确的是
A. “钡餐”中使用的硫酸钡是弱电解质
B. 镀锌铁镀层破损后,铁更容易被腐蚀
C. 提倡人们购物时不用塑料袋,是为了防止白色污染
D. 推广使用太阳能、风能、海洋能、氢能,不利于缓解温室效应
查看答案和解析>>
科目:高中化学 来源: 题型:
对于常温下pH=12的氨水,下列说法正确的是
A.由水电离产生的c(OH-)=10-12mol·L-1
B.向溶液中加入等体积的pH=2盐酸后溶液呈酸性
C.向溶液中加入稀盐酸可以促进氨水的电离,溶液的碱性增强
D.向溶液中加入适量盐酸使混合液的pH=7,混合液中c(NH4+)>c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
A.1 mol氢的质量是1 g B.1 mol CO的质量为28 g·mol-1
C.阿伏加德罗常数等于6.02×1023 D.3.01×1023个SO2分子约是0.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于蛋白质的叙述不正确的是( )
A.蛋白质溶液里加入饱和(NH4)2SO4溶液,蛋白质析出,向析出的蛋白质中加水,蛋白质不溶解
B.人工合成具有生命活力的蛋白质—结晶牛胰岛素是我国科学家在1965年首次合成的
C.重金属盐能使蛋白质凝结,故误食重金属盐会中毒
D.浓硝酸溅在皮肤上,使皮肤呈黄色,这是由于浓硝酸与蛋白质发生了颜色反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com