
 (1)中学教材上图示了NaCl晶体结构,它向三维空间延伸得到完美晶体。NiO(氧化镍)晶体结构与NaCl相同,Ni2+与最邻近的O2—的核间距离为a×10-8cm,计算NiO晶体的密度。(已知NiO的摩尔质量为:74.7g·mol-1)
(1)中学教材上图示了NaCl晶体结构,它向三维空间延伸得到完美晶体。NiO(氧化镍)晶体结构与NaCl相同,Ni2+与最邻近的O2—的核间距离为a×10-8cm,计算NiO晶体的密度。(已知NiO的摩尔质量为:74.7g·mol-1)
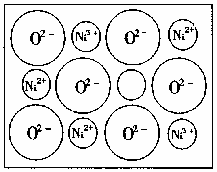
(2)天然的和大部分人工晶体都存在各种缺陷,例如在某种NiO晶体中就存在如右图所示的缺陷;一个Ni2+空缺,另有两个Ni2+被两个Ni3+所代替。其结果晶体仍呈电中性。但化合物中Ni和O的比值却发生了变化。某氧化镍样品组成为Ni0.97O,试计算该晶体中Ni3+与Ni2+的离子数之比。
科目:高中化学 来源:知识精讲与能力训练 高三化学 题型:038
(1)中学教材上图示了NaCl晶体结构,它向三维空间延伸得完美晶体.NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的核间距离为a×10-8cm.计算晶体的密度(已知NiO的摩尔质量为74.7g/mol)

(2)天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代.其结果晶体仍呈电中性,但化合物中Ni和O的比值都发生了变化.某氧化镍样品组成为:Ni0.97O,试计算该晶体中Ni3+与Ni2+的离子数之比.
查看答案和解析>>
科目:高中化学 来源: 题型:
(2)天然和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另两个被两个Ni3+所取代,但晶体仍呈现电中性,只是化合物中Ni和O的比值发生了变化。某氧化镍样品组成为Ni0.97O,试计算该晶体中Ni3+与Ni2+的离子数之比。

图3-26
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)中学教材上图示了NaCl晶体结构,它向三维空间延伸得到完美晶体。 NiO(氧化镍〕晶体的结构与NaQ相同,Ni2+与最邻近O2-的核间距离为a10-8cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7g.mol-1).
(2)天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如右图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。某氧化镍样品组成为Nio970,试计算该晶体中Ni3+与Ni2+的离子数之比。
查看答案和解析>>
科目:高中化学 来源:同步题 题型:计算题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com