
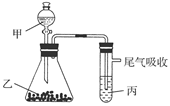
| | 甲 | 乙 | 丙 | 结论 |
| A | 水 | 电石 | 溴水 | 稳定性:水>C2H2>Br2 |
| B | 盐酸 | 石灰石 | 苯酚钠溶液 | 酸性:HCl>H2CO3>苯酚 |
| C | 盐酸 | FeS | 溴水 | 还原性:S2->Br->Cl- |
| D | 浓盐酸 | KMnO4 | KBr溶液 | 氧化性:KMnO4<Cl2<Br2 |


科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
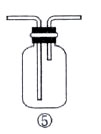
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用启普发生器制取,用排水法收集 |
| B.用启普发生器制取,用向下排空气法收集 |
| C.与加热分解KClO3制氧气的装置相同,用向下排空气法收集 |
| D.与加热分解KClO3制氧气的装置相同,用向上排空气法收集 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 物 质 |
| 沸点/℃ | 密度/g·cm-3 | ||
| 乙 醇 | -114 | 78 | 0.789 | ||
| 乙 酸 | 16.6 | 117.9 | 1.05 | ||
| 乙酸乙酯 | -83.6 | 77.5 | 0.900 | ||
| 98%H2SO4 | 10 | 338 | 1.84 |
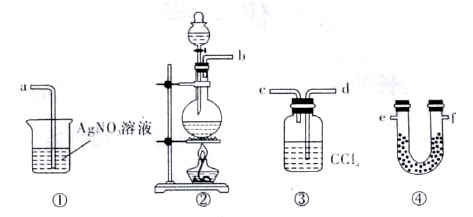
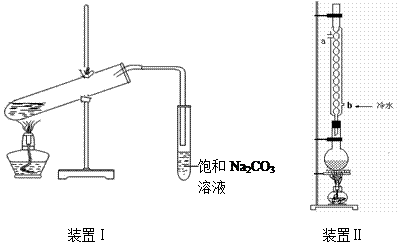
 从装置Ⅰ中右侧小试管中分离出乙酸乙酯,应进行的操作是:撤出小试管,将混合液倒入 (填仪器名称),用力振
从装置Ⅰ中右侧小试管中分离出乙酸乙酯,应进行的操作是:撤出小试管,将混合液倒入 (填仪器名称),用力振 荡,静置, (填现象),然后将产物从_____口(填“上”或“下”)倒出。
荡,静置, (填现象),然后将产物从_____口(填“上”或“下”)倒出。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
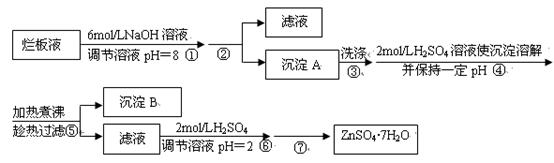
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Zn2+ | 6.4 | 8.0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

 应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。
应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
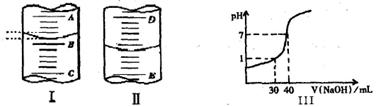
 液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)_
液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)_ _________。
_________。
 滴定后气泡消失
滴定后气泡消失查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com