
(8分)在含有弱电解质的溶液中,往往有多个化学平衡共存。
⑴现将0.04mol·L-1的HA溶液与0.02mol·L-1的NaOH溶液等体积混合。如HA是HCN,溶液中c(Na+)>c(CN-),则该混合溶液c(H+) ▲ c(OH-)(请填“>”“<”或“=”),c(HCN)+c(CN-)= ▲ mol·L-1。如HA是CH3COOH,该混合溶液呈酸性,c(CH3COOH) ▲ c(CH3COO-)(请填“>”、“<”或“=”)。
⑵常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如下图所示。回答下列问题:
①在同一溶液中,H2CO3、HCO3-、 CO32- ▲ (填:“能”或“不能”)大量共存。
②当pH=7时,溶液中各种离子其物质的量浓度之间的等量关系是: ▲ 。
⑶已知在25℃时,CO32-水解反应的平衡常数即水解常数
Kh==2×10-4,当溶c(HCO3-)︰c(CO32-)=20︰1时,溶液的pH=_▲_。
科目:高中化学 来源: 题型:
 在含有弱电解质的溶液中,往往有多个化学平衡共存.
在含有弱电解质的溶液中,往往有多个化学平衡共存.查看答案和解析>>
科目:高中化学 来源:2011-2012学年天津市蓟县一中高二第三次月考化学试卷(带解析) 题型:填空题
(选做题)(10分)在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)常温下,将0.2mol/L的某一元酸HA溶液和0.1mol/L NaOH溶液等体积混合后溶液pH大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是____
A.c(HA)<c(A-) B.c(HA)一定大于0.1mol/L
C.c(Na+)=c(HA)+c(A-) D.2c(OH-)=2c(H+)+[c(HA)-c(A-)]
(2)常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液中含碳元素的各种微粒(CO2逸出未画)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
回答下列问题:
①在同一溶液中,H2CO3、HCO3-、CO32-(填:“能”或“不能”) 大量共存。
②当pH=7时,溶液中各种离子其物质的量浓度的大小关系是:
。
③已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh= 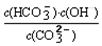 =2×10-4,当溶液中c(HCO3-)︰c(CO32-)=2︰1时,溶液的pH= 。
=2×10-4,当溶液中c(HCO3-)︰c(CO32-)=2︰1时,溶液的pH= 。
查看答案和解析>>
科目:高中化学 来源:2013届江苏省扬州市邗江区高二下学期期中考试化学试卷(解析版) 题型:填空题
(16分)在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)常温下将0.01 mol NH4Cl和0.002 mol NaOH溶于水配成1L溶液。
①溶液中浓度为0.01 mol·L-1的离子是 。
②物质的量之和为0.01 mol的两种粒子是 和 。
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 (填“碱性”、“酸性”或“中性”) ,醋酸体积 氢氧化钠溶液体积(填“>”、“<”或“=”)。
(3)将m mol·L-1的醋酸和n mol·L-1的氢氧化钠溶液等体积混合后溶液的pH=7, m与n的大小关系是m n。(填“>”、“<”或“=”)
(4)浓度为0.100 mol·L-1的下列各物质的溶液中,c( )由大到小的顺序是
)由大到小的顺序是
①NH4Cl ②NH4HSO4 ③NH3·H2O ④CH3COONH4
(5)某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A=H++HA-
HA- H++A2-
H++A2-
已知0.1 mol·L-1的NaHA溶液pH=2,则0.1 mol·L-1的H2A溶液中氢离子的物质的量浓度
0.11 mol·L-1(填“>”“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源:09-10年泰州中学高二下学期期末考试化学卷 题型:填空题
(8分)在含有弱电解质的溶液中,往往有多个化学平衡共存。
⑴现将0.04mol·L-1的HA溶液与0.02mol·L-1的NaOH溶液等体积混合。如HA是HCN,溶液中c(Na+)>c(CN-),则该混合溶液c(H+) ▲ c(OH-)(请填“>”“<”或“=”),c(HCN)+c(CN-)= ▲ mol·L-1。如HA是CH3COOH,该混合溶液呈酸性,c(CH3COOH) ▲ c(CH3COO-)(请填“>”、“<”或“=”)。
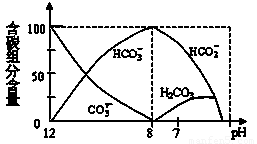
⑵常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如下图所示。回答下列问题:
①在同一溶液中,H2CO3、HCO3-、 CO32- ▲ (填:“能”或“不能”)大量共存。
②当pH=7时,溶液中各种离子其物质的量浓度之间的等量关系是: ▲ 。
⑶已知在25℃时,CO32-水解反应的平衡常数即水解常数
Kh==2×10-4,当溶c(HCO3-)︰c(CO32-)=20︰1时,溶液的pH=_▲_。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com