
| A、澄清石灰水与稀盐酸反应 Ca(OH)2+2H+=Ca2++2H20 |
| B、碳酸钠溶液与盐酸反应 Na2CO3+2H+?=2Na++H2O+CO2↑ |
| C、稀硫酸与氢氧化钡溶液反应 H++OH-+Ba2++SO42-=H2O+BaSO4↓ |
| D、氢氧化铜与稀硫酸反应 Cu(OH)2+2H+=Cu2++2H2O |


科目:高中化学 来源: 题型:
| A、将碘水倒入分液漏斗,加适量乙醇,震荡后静置,能将碘萃取到乙醇中 |
| B、用湿润的pH试纸测定溶液的pH,测定结果偏小,该溶液一定呈酸性 |
| C、向某溶液中加入K3[Fe(CN)6]溶液,生成特征蓝色的沉淀,原溶液中含有Fe2+ |
| D、在含有FeCl2杂质的FeCl3溶液中通入足量的Cl2后,充分加热蒸干,可得到纯净的FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫黄是一种易溶于水的黄色晶体 |
| B、SO2的水溶液显酸性 |
| C、SO2是黄色易溶于水的有毒气体 |
| D、SO2不稳定,极易转化为SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在硫氢化钠溶液中加入稀硫酸溶液:S2-+2H+→H2S↑ |
| B、用氢氧化钠溶液除去镁粉中的铝粉:2Al+2OH-→AlO2-+H2↑ |
| C、向碳酸氢钠溶液中加入少量氢氧化钙溶液:2HCO3-+Ca2++2OH-→CaCO3↓+CO32-+2H2O |
| D、偏铝酸钠溶液中通入少量二氧化碳:2AlO2-+CO2+3H2O→2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
| B、可以用Si3N4、Al2O3制作高温结构陶瓷制品 |
| C、地球上CH4、CO2等气体含量上升容易导致温室效应加剧,进而引发灾难性气候 |
| D、禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
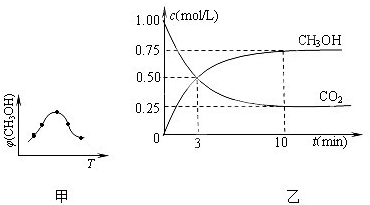
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com